
China
Borran en embriones enfermedades hereditarias
Un equipo internacional de científicos logra por primera vez corregir en embriones la mutación del gen que causa miocardiopatía hipertrófica, una enfermedad hereditaria que afecta a una de cada 500 personas
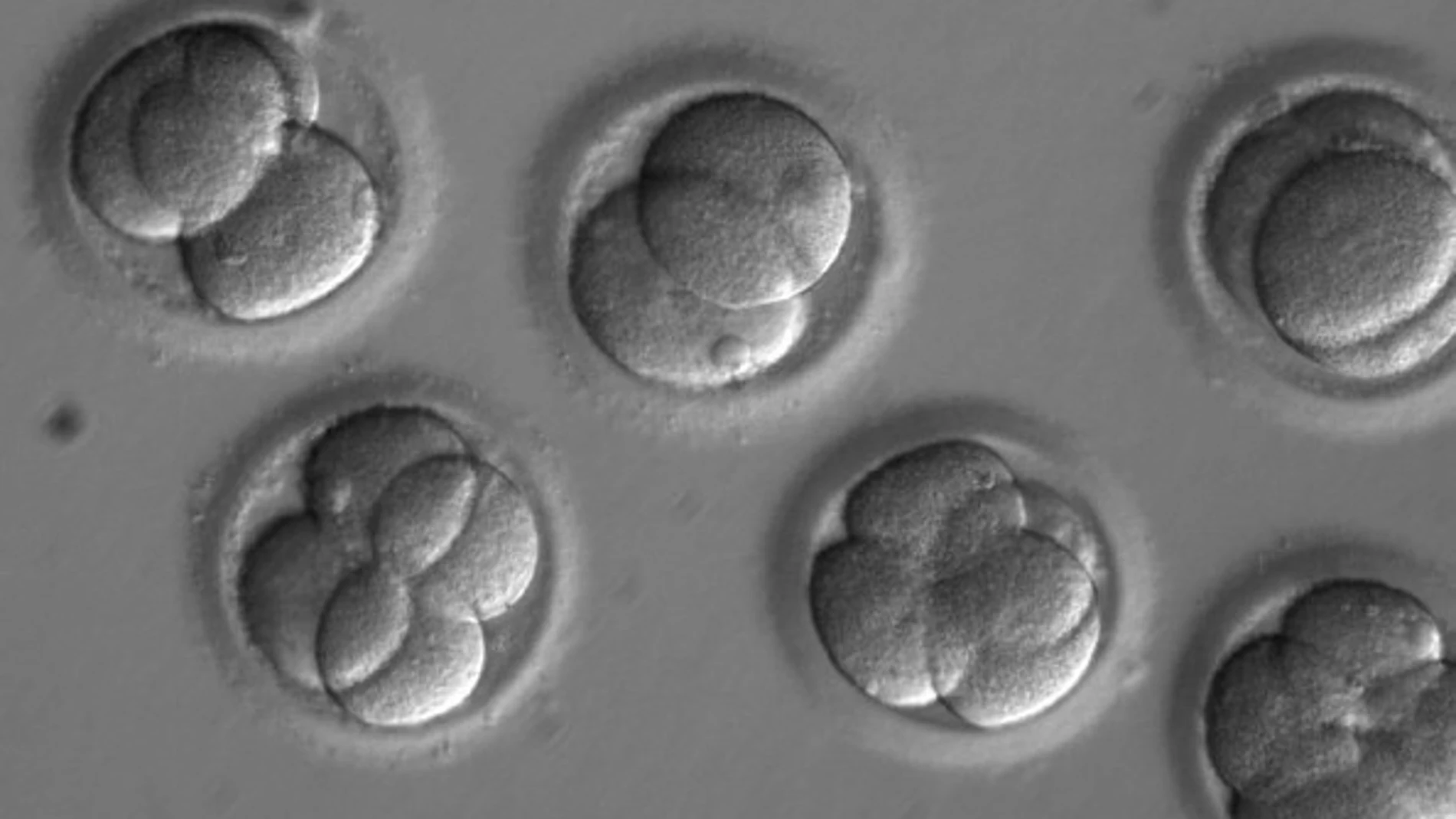
Un equipo internacional de científicos, entre ellos Juan Carlos Izpisúa, ha logrado, por primera vez, eliminar una patología gracias a la técnica de «corta y pega» genético. España, al firmar el Protocolo de Oviedo, no permite realizar este tipo de investigación.
Un grupo de científicos internacionales, entre los que se encuentra el español Juan Carlos Izpisúa, ha conseguido por primera vez, borrar una enfermedad hereditaria en embriones humanos. La técnica, que utiliza el sistema CRISPR-Cas9, permite corregir la mutación genética que provoca una afección cardíaca frecuente, la miocardiopatía hipertrófica, la causa más común de muerte súbita en atletas jóvenes sanos que afecta a 1 de cada 500 personas.
Esta enfermedad se origina por una mutación en el gen MYBPC3, pero a menudo pasa desapercibida hasta que es demasiado tarde. Dado que las personas con una copia mutada de este gen tienen un 50% de probabilidades de transmitirlo a sus hijos, corregir esta modificación en los embriones evitaría la enfermedad no sólo en los niños afectados, sino también en sus descendientes.
Pero esta investigación va más allá. Es toda una revolución en el campo de la Medicina y de la Ciencia puesto que abre la puerta al tratamiento de muchas patologías consideradas raras y de ciertos tipos de cáncer causados por la mutación defectuosa de algún gen.
El trabajo, publicado ayer en la revista «Nature», es una colaboración entre el Instituto Salk de California, la Universidad de Salud y Ciencias de Oregón (OHSU) y el Instituto Coreano de Ciencias Básicas. «Gracias a los avances en las tecnologías de células madre y la edición de genes estamos empezando a tratar las mutaciones causantes de enfermedades que afectan a millones de personas», dice Juan Carlos Izpisua Belmonte, profesor del Laboratorio de Expresión Genética de Salk y uno de los autores. Aunque advierte que, «la edición de genes todavía está en una fase muy temprana, así que, aunque este trabajo preliminar es seguro y eficaz, es crucial que sigamos actuando con la mayor precaución, prestando la máxima atención a las consideraciones éticas». Cabe recordar que el estudio cumple plenamente con las directrices éticas establecidas por la Academia Nacional de Ciencias de EE UU.
Para llevarlo a cabo, los investigadores generaron células madre pluripotenciales extraídas a partir de una biopsia de piel donada por un varón con miocardiopatía hipertrófica y desarrollaron una estrategia de edición de genes con la técnica CRISPR-Cas9 para reparar la copia mutada del gen MYBPC3. El gen defectuoso fue cortado por la enzima Cas9 y permitió que los mecanismos de reparación de ADN de las células del donante eliminaran la mutación durante la siguiente ronda de división celular e introducirlo en un espermatozoide donado por el mismo hombre. Con técnicas de inseminación in vitro, inyectaron esta modificación en óvulos de mujeres sanas. Luego analizaron todas las células en los primeros embriones para comprobara que la mutación se había reparado.
«Después de que CRISPR hiciera el corte, el embrión inició sus propias reparaciones, pero en lugar de utilizar la plantilla de ADN sintético suministrada lo hizo usando preferentemente la copia saludable del gen aportada por la madre, lo que fue una sorpresa», señala en una nota del Instituto Salk Jun Wu, otro de los firmantes. No solo se repararon un alto porcentaje de células embrionarias, sino que la corrección no indujo otras mutaciones ni inestabilidad en el genoma: lograron que el 72 % de los embriones portaran dos copias sanas del gen.
Al margen del éxito, los investigadores puntualizaron que los enfoques de edición del genoma deben ser optimizados antes de pasar a los ensayos clínicos. «Esta investigación avanza significativamente la comprensión científica de los procedimientos que serían necesarios para garantizar la seguridad y la eficacia de la corrección genética», explica Daniel Dorsa, vicepresidente senior de investigación de OHSU. y añade que «las consideraciones éticas de trasladar esta tecnología a ensayos clínicos son complejas y merecen un compromiso público significativo antes de que podamos responder a la pregunta más amplia de si es de interés para la humanidad alterar los genes humanos para las generaciones futuras».
Este estudio proporciona una nueva visión de una técnica que podría aplicarse a miles de trastornos genéticos hereditarios que afectan a millones de personas en todo el mundo. También podría aumentar el éxito de los procesos de inseminación al aumentar el número de embriones sanos. «Si conseguimos confirmar su seguridad, esta técnica podría potencialmente disminuir el número de ciclos necesarios para las personas que tratan de tener hijos libres de enfermedad genética», añade Paula Amato, otra de las autoras y profesora asociada de Obstetricia y Ginecología en la Escuela de Medicina de OHSU.
Esta técnica sería iniviable en nuestro país en este momento, ya que el Protocolo de Oviedo, firmado por 29 países, entre ellos España, no permite crear embriones para investigación y sólo se podrían utilizar los desechados de ciclos de fecundación.
✕
Accede a tu cuenta para comentar


