Investigación
Una prometedora terapia "in vitro" española logra mayor muerte tumoral con menos quimioterapia
Combina dos tipos de calor local, hipertermia magnética y radiación infrarroja, con el medicamento doxorrubicina para atacar el cáncer con mayor precisión y menor toxicidad
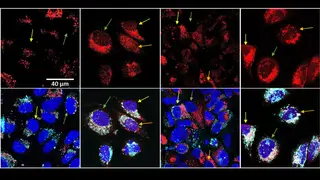
Un equipo del Instituto de Ciencia de Materiales de Madrid (ICMM‑CSIC) ha logrado un avance significativo en la investigación oncológica al desarrollar una estrategia innovadora que combina quimioterapia y dos tipos distintos de calor local para potenciar la destrucción de células tumorales. El estudio, realizado en colaboración con instituciones de Francia y España, ha sido seleccionado como portada en la revista Advanced NanoBiomed Research, lo que subraya su relevancia científica y su potencial clínico.
La propuesta, aún en fase experimental, se basa en una terapia trimodal que integra tres elementos: nanopartículas magnéticas capaces de transportar el fármaco doxorrubicina -uno de los quimioterápicos más utilizados-; hipertermia magnética, producida mediante un campo magnético alterno; y terapia fototérmica, que emplea radiación en el infrarrojo cercano. La combinación simultánea de estos tres mecanismos permite atacar el tumor desde distintas vías, incrementando la eficacia y reduciendo la toxicidad asociada a la quimioterapia tradicional.
Según los investigadores, liderados por la científica Ana Espinosa, las nanopartículas están diseñadas para liberar la doxorrubicina solo cuando se calientan, un proceso activado por las dos fuentes de hipertermia. Esta liberación controlada, además de localizar el tratamiento en la zona tumoral, evita la exposición innecesaria de los tejidos sanos al fármaco,minimizando así los efectos secundarios sistémicos que suelen limitar las dosis en la práctica clínica.
Hasta un 70% de muerte celular en tres días
Los experimentos, realizados en cultivos celulares de cáncer de mama, muestran que esta estrategia logra hasta un 70% de muerte celular a las 72 horas, un porcentaje significativamente superior al de los tratamientos individuales. Uno de los factores clave es que las células tumorales son especialmente vulnerables a las altas temperaturas; sin embargo, alcanzar los niveles necesarios de calor de forma segura es complicado si se utiliza únicamente uno de los métodos térmicos. De ahí la importancia de la combinación: mientras cada fuente de calor por separado resulta insuficiente o excesivamente agresiva, juntas permiten alcanzar la temperatura terapéutica con intensidades más bajas y seguras.
El estudio describe en detalle las nanopartículas utilizadas, que están compuestas por óxido de hierro, un material biocompatible que el organismo puede degradar de manera natural. Su tamaño -miles de veces menor que el grosor de un cabello- facilita su internalización en las células tumorales y su respuesta eficiente tanto al campo magnético como a la radiación infrarroja. Además, la doxorrubicina se incorpora mediante interacciones químicas que garantizan un transporte estable y una liberación sensible al pH ácido característico de los tumores, lo que añade otra capa de precisión al tratamiento.
La investigación también confirma, mediante técnicas avanzadas de caracterización, que las nanopartículas mantienen su estructura durante los procesos térmicos, un aspecto esencial para su viabilidad. Ensayos citotóxicos realizados en paralelo muestran que la combinación de hipertermia magnética y fototérmica mejora la eficacia respecto a la doxorrubicina libre, incluso cuando se emplean dosis más bajas de este fármaco, algo especialmente relevante para reducir efectos adversos.
Una "trampa de calor"
Los investigadores destacan que el objetivo es crear una "trampa de calor” dentro del tumor, activando simultáneamente la quimioterapia localizada y las dos formas de hipertermia para maximizar el daño celular mientras se protege el tejido sano. Si la estrategia demuestra su eficacia en modelos animales y posteriores ensayos clínicos, podría convertirse en una alternativa real para reducir las dosis de quimioterapia y mejorar la calidad de vida de los pacientes.
El trabajo, desarrollado en colaboración con IMDEA Nanociencia, el Instituto Curie (Francia) y el Instituto de Cerámica y Vidrio (ICV‑CSIC), abre una vía prometedora hacia terapias oncológicas más específicas, menos invasivas y potencialmente aplicables a múltiples tipos de tumor. Aunque los resultados obtenidos son exclusivamente "in vitro", los autores subrayan que el enfoque es escalable y podría adaptarse a estudios preclínicos más avanzados.

