
Investigación científica
Errores y aciertos en el campo del alzhéimer
El próximo miércoles se celebra el Día Mundial de esta patología neurodegenerativa y toca hacer balance de los últimos diez años: se han sentado las bases para una prevención eficaz a través de la dieta y el ejercicio y un diagnóstico temprano gracias a biomarcadores y los avances de la neuroimagen, pero siguen las incógnitas a la hora de encontrar una terapia eficaz
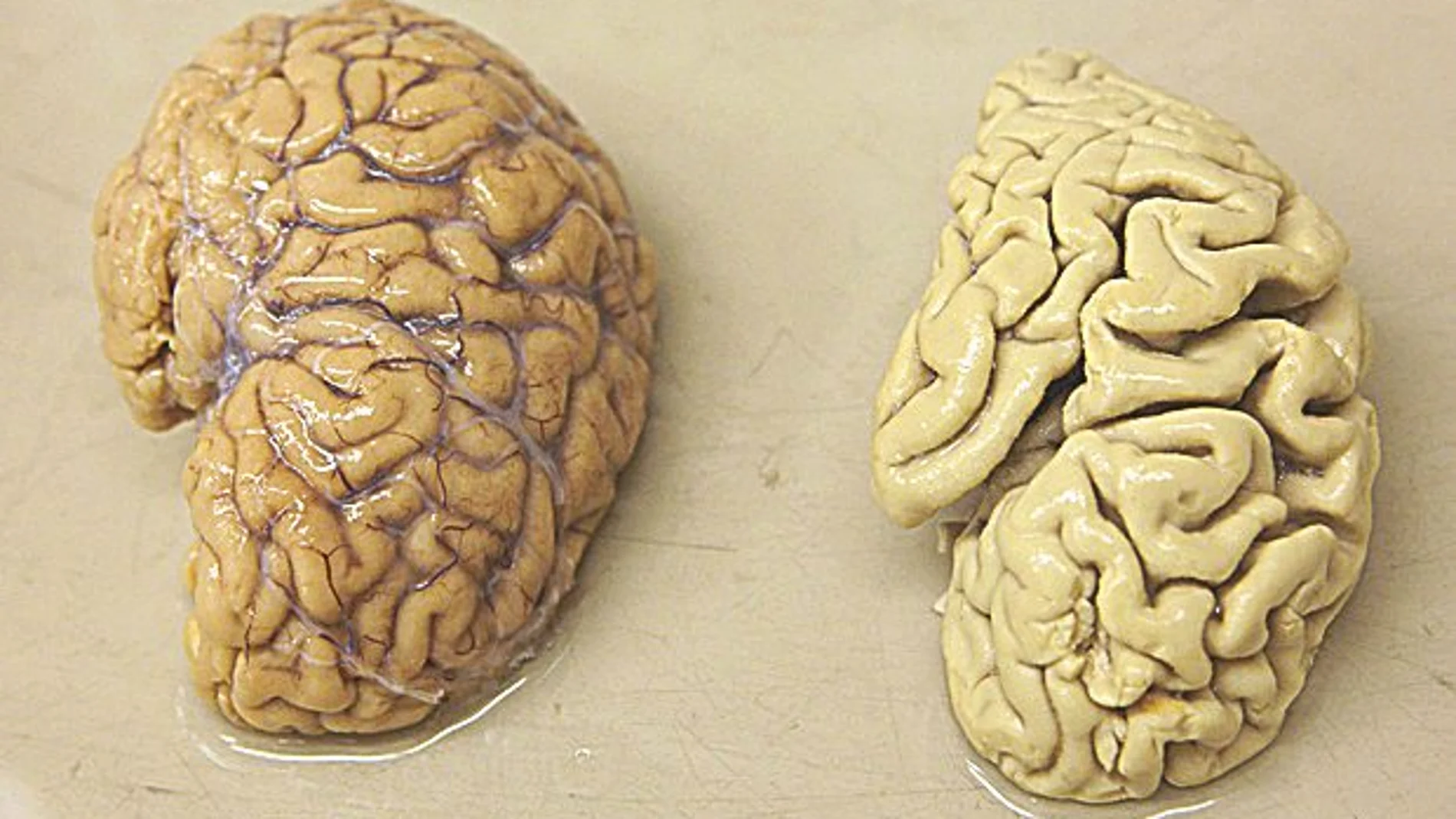
El próximo miércoles se celebra el Día Mundial de esta patología neurodegenerativa y toca hacer balance de los últimos diez años
Esperanza, para muchos es lo último que se pierde. Más aún para los tres millones de españoles, entre pacientes y familiares, que conviven cada día con las consecuencias devastadoras del alzhéimer. «Queremos encontrar una solución, pero mientras tanto no podemos dar falsas expectativas a los afectados. De los 15 minutos que dedico en mi consulta, ¿se puede hacer una idea de la cantidad de veces que he tenido que explicar en los últimos 15 días que el último fármaco que ha sido noticia –aducanumab– aún no está disponible? Es duro para ellos asumir que no hay cura», explica Alberto Villarejo, vocal del Grupo de Estudio de Conducta y Demencias de la Sociedad Española de Neurología (SEN).
Con el fin de encontrar respuestas sólidas para los pacientes, A TU SALUD se ha consultado a un nutrido grupo de expertos para que expliquen cómo está la situación y hagan un repaso a los errores y aciertos de la última década. Aquí, uno de los puntos que más preocupan a los especialistas es que «seguimos sin conocer las causas ni los mecanismos concretos que desencadenan la enfermedad», subraya Eva Carro, miembro del Grupo de Enfermedades Neurodegenerativas del Instituto de Investigación Hospital 12 de Octubre en Madrid.
Villarejo puntualiza que «pese a que sabemos que el origen pasa por la acumulación de la beta amiloide y la alteración de la proteína Tau, en realidad no conocemos sus funciones biológicas en el organismo. Aquí es necesaria más investigación básica». Algo tan esencial como conocer qué hacen y no sólo saber de ellas cuando están mal. «Un problema importante deriva precisamente de esta complejidad en múltiples niveles, que genera una inmensidad de datos difíciles de integrar en modelos que sean útiles desde el punto de vista terapéutico. Varios proyectos internacionales de gran envergadura, como el ‘‘Human Brain Project’’ europeo o la ‘‘Brain Initiative’’ norteamericana, están dirigidos a lograr esa difícil integración. Otro problema fundamental deriva de la complejidad de las causas de la enfermedad de Alzheimer, que se encuentran estrechamente relacionadas con el proceso de envejecimiento cerebral y los mecanismos naturales compensatorios que desencadena», explica Alberto Rábano, director del Banco de Tejidos de Fundación del Centro de Investigación de Enfermedades neurológicas (CIEN).
Con lo que se sabe hoy de la enfermedad neurodegenerativa, Rafael Blesa, jefe del Servicio de Neurología del Hospital de la Santa Creu i Sant Pau y de la UAB, manifiesta que «las grandes oportunidades que ahora se nos plantean son: uno, la prevención: evitando el depósito de amiloide; y dos, la curación: siendo capaces de frenar los síntomas combatiendo la presencia de la Tau». En este sentido, Blesa añade que «tenemos dos grandes incógnitas que no hemos resuelto: el mecanismo por el que la acumulación de amiloide dispara la muerte neuronal y la aparición de la proteína Tau. Tampoco hemos sabido encontrar la diana terapéutica adecuada (han fracasado el 100% de los más de 500 ensayos clínicos farmacológicos que se han realizado en los últimos 14 años)». ¿Por qué?¿Qué ha impedido que no haya llegado una solución terapéutica efectiva?
¿Para cuándo una cura?
La mayoría de los consultados tienen claro qué ha fallado. Y la mayoría apunta al mal diseño de los ensayos clínicos, a la obsesión de encontrar resultados en los pacientes más avanzados. José Luis Molinuevo, de la Unidad de Alzhéimer y otros desórdenes cognitivos del Servicio de Neurología del ICN Hospital Clínic de Barcelona y director científico de la Fundación Pasqual Maragall, explica que «en los últimos años se ha llevado a cabo una reconceptualización de la enfermedad a nivel terapéutico. Sabemos que hay que actuar contra las proteínas, que tienen un rol importante. Pero no sobre la enfermedad más grave, sino en pacientes con signos leves. En este sentido, destaca el estudio reciente de ‘‘The Lancet’’, que ha conseguido buenos resultados. Se han observado cambios clínicos en los pacientes y hay evidencias ‘‘in vivo’’ de que vamos bien en cuanto a la etiología».
A esto, Jesús Ávila, del Centro de Biología Molecular Severo Ochoa y del Centro Superior de Investigaciones Científicas (CSIC), añade otro motivo: «Quizás se simplificó mucho como factor de riesgo el péptido amiloide, como casi única diana de la enfermedad». En esta línea, coincide con Ramón Cacabelos, catedrático en Medicina Genómica y presidente del grupo de investigación biomédica Euroespes que desarrolla la idea: «la persistencia en el hecho de que el alzhéimer es exclusivamente una amidolopatía ha sido un error, ya que se ha focalizado todo el interés fotopatogénico y terapéutico en la misma dirección». Por ello, para el portavoz del CSIC está claro cuál es la nueva senda: «Empezamos buscando curación, luego prevención y ahora, el retraso de la aparición de la enfermedad. Quizás con este cambio podemos ir prosperando mejor».
Pero no todo está perdido. Aunque la cura no esté aquí hoy, los avances apuntan a que en diez años ya habrá armas moleculares para, al menos, si no curar, retrasar e incluso frenar, los síntomas de la neurodegeneración. «Hay varias líneas de tratamiento que pueden resultar útiles, aunque la eficacia final dependerá sin duda del momento en que se aplique el tratamiento. Lo ideal es que se pudiera aplicar antes de que aparezcan los síntomas o cuando sólo han aparecido síntomas ligeros, porque sabemos que cuando el deterioro cognitivo y funcional es importante ya han desaparecido muchos millones de neuronas que no podrán ser restituidas», apunta Rábano.
López Sousa comenta que «la esperanza está dirigida a las sustancias que actúan sobre el beta-amiloide, en forma de vacunas, mediante anticuerpos e inhibidores o moduladores de la secretasa, así como agentes dirigidos contra la proteína Tau y compuestos que actúan como antagonistas de otros sistemas de neurotransmisores, tanto serotoninérgicos como histaminérgicos». Aquí destacan como prometedores, como coinciden en su apunte muchos de los expertos, los ensayos clínicos con aducanumab (el que publicó sus resultados en «The Lancet» hace dos semanas), solanezumab, gantenerumab y crenezumab, «en la actualidad parecen los más prometedores. Aunque también se están analizando otras vías terapéuticas a través de vacunas dirigidas contra las otras dianas, como es la proteína Tau», añade López Sousa.
Mientras todo esto llega, la mejor forma de combatirlo es la prevención. Blesa lamenta que «no es de recibo que España sea uno de los pocos países desarrollados que no haya creado un Plan Nacional Alzheimer. Hemos de conseguir que el próximo gobierno lo desarrolle». Su postura está respaldada por la opinión de sus compañeros, puesto que Villarejo subraya que «hay estrategias, pero no hay algo que comprometa a la acción. Si hay un plan nacional se rinden cuentas y eso es necesario para luchar contra la enfermedad desde todos los puntos de vista». Así, si la prevención es una arma efectiva, «llama la atención la poca sensibilidad política que ha existido en cuanto a una prevención desde la infancia, donde debería ser reforzada. Si sabemos que lo bueno para el corazón también lo es para el cerebro, por qué permitir índices de obesidad, tabaco y alcohol tan altos en los jóvenes», concluye Blesa.
El origen: la gran incógnita
«Desde la primera descripción de la enfermedad de Alzheimer en el año 1907 se han establecido muchas hipótesis para explicar su etiología pero todavía no tenemos certeza absoluta de cómo se produce», explica Secundino López Pousa, coordinador del servicio de Neurología de los hospitales Josep Trueta de Girona y Santa Caterina de Sal. Blesa apunta que «desgraciadamente lo conocemos todo acerca del proceso de deterioro cognitivo y funcional que sufre la persona afectada de alzhéimer, como también sabemos hasta qué punto esta enfermedad es cruel para con la familia y los cuidadores del enfermo». Después de tres décadas de estudios genéticos, «se ha descubierto que aproximadamente el 5% de los casos son claramente por trasmisión genética, y que éstos se desarrollan generalmente en edades jóvenes, prensiles. Por lo tanto la mayoría de los casos de la enfermedad de Alzheimer se desarrollan en edades avanzadas, después de los 65 años, y para estos casos el factor de riesgo más conocido hasta ahora sigue siendo una alteración genética ligada a una lipoproteína (APOE), que condicionada a la gestión del alelo 4, aumenta el riesgo de subir la enfermedad entre 3 y 10 veces, dependiendo de la carga de este alelo. Aun así, la presencia de este alelo sólo explica el 50% de los casos, lo que indica que existen otros factores de riesgos genéticos o medioambientales desconocidos que también están implicados en el desarrollo del proceso. A pesar de que en los últimos diez años se han analizado millones de muestras sanguíneas para conocer aspectos genéticos específicos, en la práctica clínica estos hallazgos han tenido poca trascendencia y no han modificado el manejo de la enfermedad», concluye López Pousa.
✕
Accede a tu cuenta para comentar


