
Salud
La solución a los stents obstruidos
Científicos españoles descubren dos proteínas implicadas en la oclusión de estos dispositivos
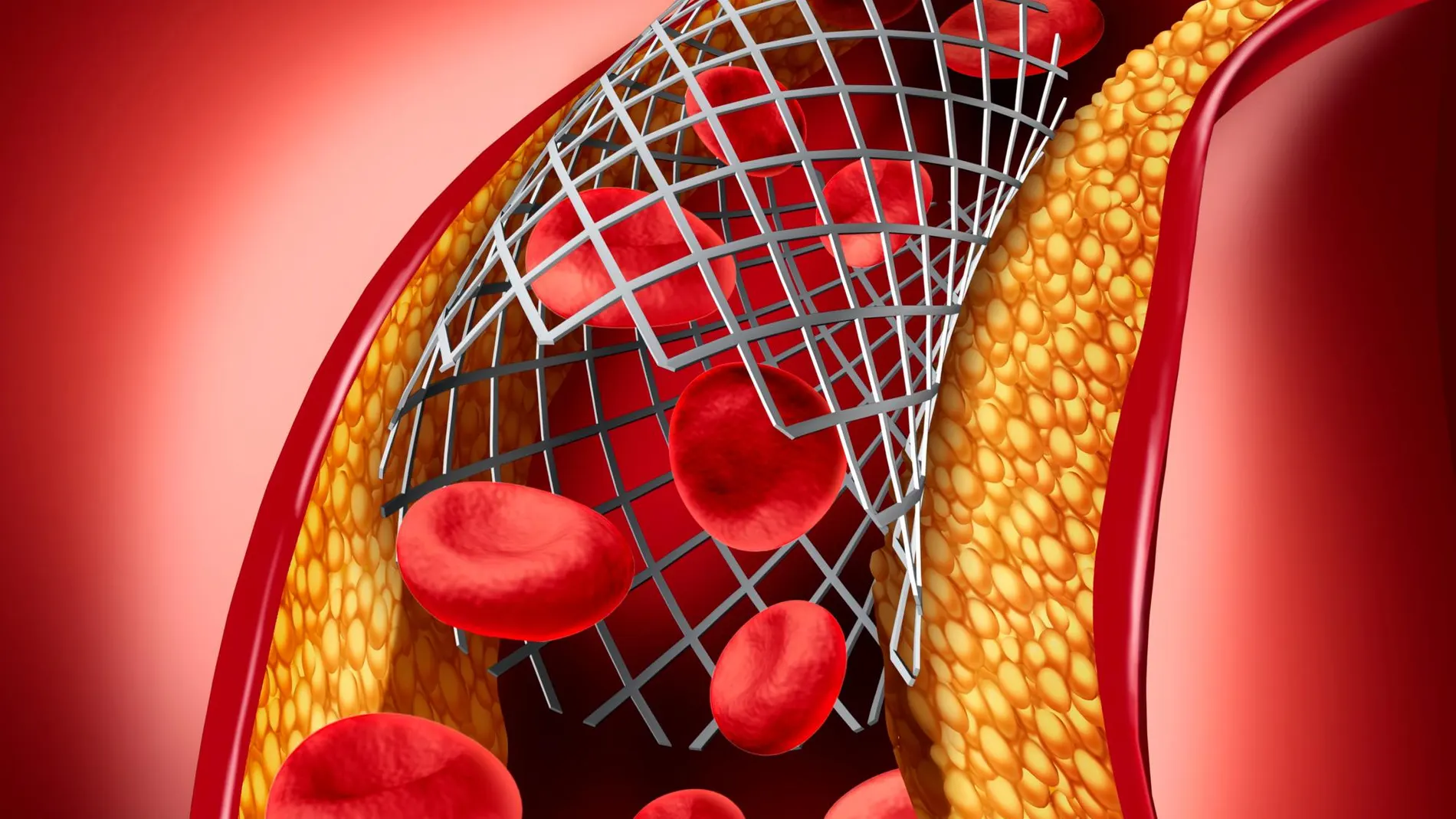
Científicos españoles descubren dos proteínas implicadas en la oclusión de estos dispositivos
La enfermedad arterial coronaria es la principal causa de muerte en los países occidentales. Esta enfermedad está causada, generalmente, por la aterosclerosis, una patología crónica caracterizada por la acumulación progresiva de colesterol y células del sistema inmune en la pared arterial que, al formar una placa aterosclerótica, obstruye las arterias y puede provocar la muerte debido a una angina o un infarto de miocardio.
Aunque el tratamiento de la enfermedad arterialcoronaria se basa en cambios en el estilo de vida más saludables y la administración de distintos fármacos, cuando la enfermedad progresa y se produce una oclusión importante de las arterias coronarias es necesario un tratamiento de revascularización mediante cirugía cardiaca o intervencionismo coronario percutáneo, un procedimiento que consiste en la dilatación de la arteria con un balón y el implante de un stent (prótesis cilíndrica de metal) en el lugar de la obstrucción.
El problema es que, en ocasiones, éste puede fallar debido a un proceso denominado reestenosis, que consiste en la proliferación de células de músculo liso de la pared arterial que pueden llegar a taponar el stent.
Esta circunstancia puede suceder en todas las personas. Sin embargo, hay que tener en cuenta que existen diferentes factores de riesgo que favorecen la restenosis como la diabetes, sexo femenino, tipo y número de stents colocados, longitud de la lesión y colocación en vasos de pequeño calibre.
Aunque esta reestenosis puede controlarse mediante el uso de stents liberadores de fármacos, en el 10% de los casos sigue produciendo el fallo del stent, siendo un problema clínico aún por resolver.
Para intentar paliar este problema, investigadores del Ciber de Enfermedades Cardiovasculares (CiberCV) en el Instituto de Investigación Sanitaria de la Fundación Jiménez Díaz (IIS-FJD) de Madrid han descubierto un nuevo mecanismo implicado en este proceso de reestenosis post-angioplastia. Estos resultados han permitido identificar una posible terapia para esta patología.
Nuevas terapias
“Nuestro estudio demuestra que la interacción de dos proteínas denominadas Tweak y Fn14 inducen la proliferación de la célula de músculo liso de la pared arterial. Así, tras realizar una angioplastia en la arteria, la interacción de estas dos proteínas que inhiben la proliferación celular, favoreciéndola y contribuyendo a la reestenosis y, en último término, al fallo del stent implantado”, explica Luis Miguel Blanco-Colio, quien ha liderado este trabajo.
En este trabajo, en el que han participado también investigadores del CiberDEM (Ciber de Diabetes y Enfermedades Metabólicas Asociadas) y otras instituciones a nivel internacional, se desvela el mecanismo molecular, hasta ahora desconocido, por el que estas dos proteínas controlan la proliferación celular. Concretamente, se demuestra que el eje Tweak/Fn14 controla la expresión de un gen supresor de tumores, el p15INK4B, que participa en el mantenimiento del estado de reposo en diferentes células.
“En este estudio hemos demostrado en animales modificados genéticamente, que el eje Tweak/Fn14 juega un papel fundamental en la formación de la lesión reestenótica tras una angioplastia in vivo, al disminuir la expresión de p15INK4B con el consiguiente aumento de la proliferación celular”, indica la primera firmante del trabajo, Nerea Méndez-Barbero.
La identificación de mecanismos asociados a la reestenosis post-angioplastia podría facilitar el desarrollo de fármacos útiles para el tratamiento de esta patología cardiovascular.
“En la actualidad existen stents que liberan fármacos de una manera local. En nuestro estudio hemos demostrado que el uso de un anticuerpo humanizado anti-Tweak es capaz de disminuir el porcentaje de restenosis tras una angioplastia. Por lo tanto, el uso de stents con inhibidores específicos de estas proteínas podría ser una estrategia beneficiosa para reducir la aparición de reestenosis», asegura Blanco-Colio.
No obstante, y pese a lo novedoso de los resultados obtenidos en su investigación, advierte de la importancia de tomarlos “con cautela, ya que no siempre lo que observamos en ratones tiene el mismo efecto en humanos. El siguiente paso debería ser analizar el resultado de la inhibición de estas proteínas sobre la reestenosis en animales superiores para confirmar que el mecanismo de acción no es específico de ratones”.
✕
Accede a tu cuenta para comentar


