
Investigación científica
¿Por qué el corazón de los adultos se regenera peor que el de los bebés?
El hallazgo de la causa podría contribuir al desarrollo de nuevas estrategias que puedan servir para la recuperación de corazones infartados
El hallazgo de la causa podría contribuir al desarrollo de nuevas estrategias que puedan servir para la recuperación de corazones infartados
El infarto de miocardio es una patología propia de personas de cierta edad. En concreto de personas que han dejado de ser bebés. Durante las primeras fases de desarrollo postnatal, los recién nacidos conservan una asombrosa capacidad de regeneración de algunas de sus células cardiacas. En concreto, pueden generar nuevos cardiomiocitos (las células del músculo cardiaco que son capaces de contraerse y hacer que funcione el corazón). Al menos en los primeros meses de vida, los mamíferos pueden autorreparar un miocardio dañado porque sus cardiomiocitos no dejan de dividirse. Pero con el paso del tiempo esta función se deteriora. En la edad adulta, la tasa de reparación de cardiomiocitos tras un infarto no llega al uno por ciento anual. Insuficiente para devolver al órgano a su estado sano si el daño ha sido severo.
Desde hace tiempo se sabe que hay un momento clave en el desarrollo del músculo cardiaco a partir del cual las células no son capaces de regenerarse más. ¿Pero de qué depende ese momento? ¿Qué mecanismos biológicos están implicados en la pérdida de esta habilidad?
Una investigación llevada a cabo por científicos del Centro Nacional de Investigaciones Cardiovasculares Carlos III (CNIC) de Madrid puede arrojar luz sobre estas preguntas. En concreto, según se publicó ayer en la revista The Journal of Cell Biology, la capacidad de renovación de los cardiomiocitos depende de la longitud de los telómeros.
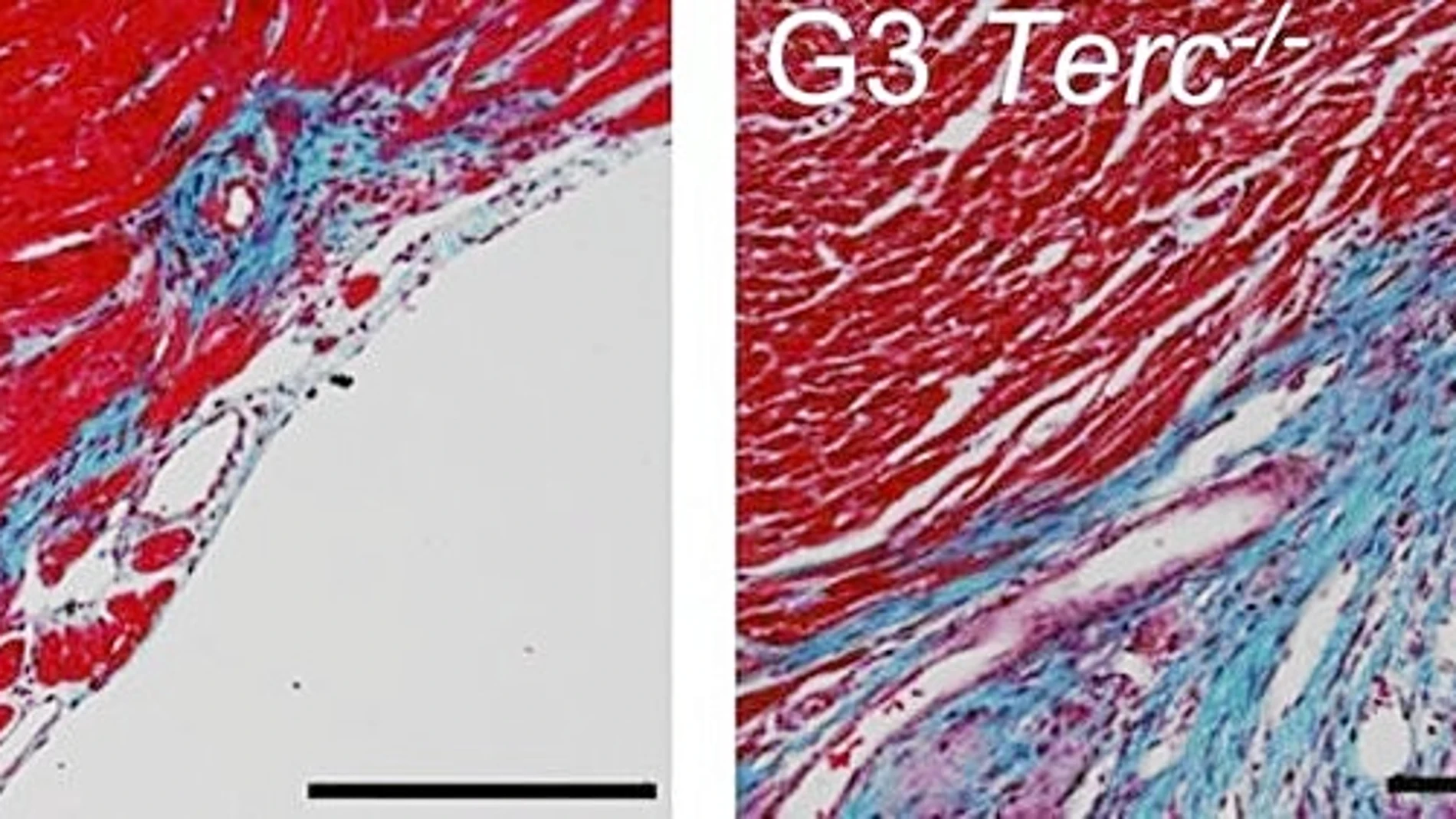
Los telómeros son estructuras localizadas en el extremo de los cromosomas. Sirven para mantener la estabilidad estructural de estos paquetes de ADN que contienen la mayor parte de nuestra información genética y que están presentes en nuestras células. Son como los herretes de plástico o metal que se pone a los cordones de los zapatos para que no se deshilachen. Sabemos que los telómeros, en concreto su acortamiento con el paso del tiempo, están relacionados con muchos procesos biológicos como el envejecimiento celular o incluso algunos tipos de cáncer. Pero esta nueva investigación parece confirmar que también intervienen en la capacidad de regeneración del músculo cardiaco. El equipo del CNIC, dirigido por el doctor Ignacio Flores, ha analizado los mecanismos moleculares que intervienen en el desarrollo del corazón de ratones en sus primeros días de vida en busca de una razón que explique por qué los cardiomiocitos dejan de dividirse en un momento dado. Y ha descubierto, precisamente, que los telómeros se acortan de manera repentina poco tiempo después del nacimiento. Eso genera que los extremos de los cromosomas sean reconocidos como «puntos de daño» en el ADN y se deteriore el correcto funcionamiento del ciclo celular. Los investigadores utilizaron como modelo diferentes tipos de ratones, algunos de los cuales carecían de telomerasa, la enzima encargada de alargar los telómeros. Estos animales en los que la telomerasa estaba ausente presentaban un acortamiento prematuro de sus telómeros. Esta respuesta parecía esperable. Pero, ¿tendría algo que ver con la pérdida de capacidad regeneradora del músculo cardiaco? El siguiente paso fue provocar daño cardiaco a los ratones con un día de vida y observar su evolución. Efectivamente, los animales con los telómeros más acortados tuvieron más dificultades para regenerar su corazón: se comportaban de manera más parecida a como lo hace un ratón adulto.
Pero la investigación ha ido más allá. Se ha descubierto que los animales con telómeros acortados en sus cardiomiocitos presentan un aumento en los niveles de la proteína p21, una sustancia que provoca la parada del ciclo celular. De hecho, cuando se inhibió esta proteína los cardiomiocitos volvían a dividirse, aunque tuvieran sus telómeros excepcionalmente cortos. Es decir, se ha confirmado que el tamaño de los telómeros es una de las causas que hay detrás de la pérdida de capacidad regeneradora del músculo cardiaco y la proteína p21 está presente en el proceso. No es la única. En palabras de propio doctor Flores, «no se descarta la existencia de otros factores que también podrían contribuir a la inhibición de la proliferación en este tipo celular». Este trabajo «apunta a que preservar la longitud y la función de los telómeros en una subpoblación de cardiomiocitos podría ser importante de cara a aumentar la capacidad regenerativa del corazón adulto, por ejemplo, después de un infarto de miocardio» declara Flores a LA RAZÓN. Es decir, podría haberse abierto la puerta a una nueva estrategia de contención o de prevención de la enfermedad cardiaca más común: la vigilancia y el mantenimiento de las reservas de telómeros suficientemente funcionales.
Flores recuerda que los componentes y la regulación del ciclo celular en células de ratón difieren mínimamente de los componentes y la regulación del ciclo celular en células humanas por lo que la investigación con estos animales es de gran relevancia.
✕
Accede a tu cuenta para comentar


