
Investigación científica
El exceso de amoníaco en la sangre eleva la mortalidad neonatal
El niño que nace con un trastorno del ciclo de la urea está aparentemente sano, pero con el paso de las horas, el amoníaco se acumula en su sangre y provoca daños en el sistema nervioso central que son irreversibles. Hasta el 50% muere antes de recibir diagnóstico, con apenas semanas de vida
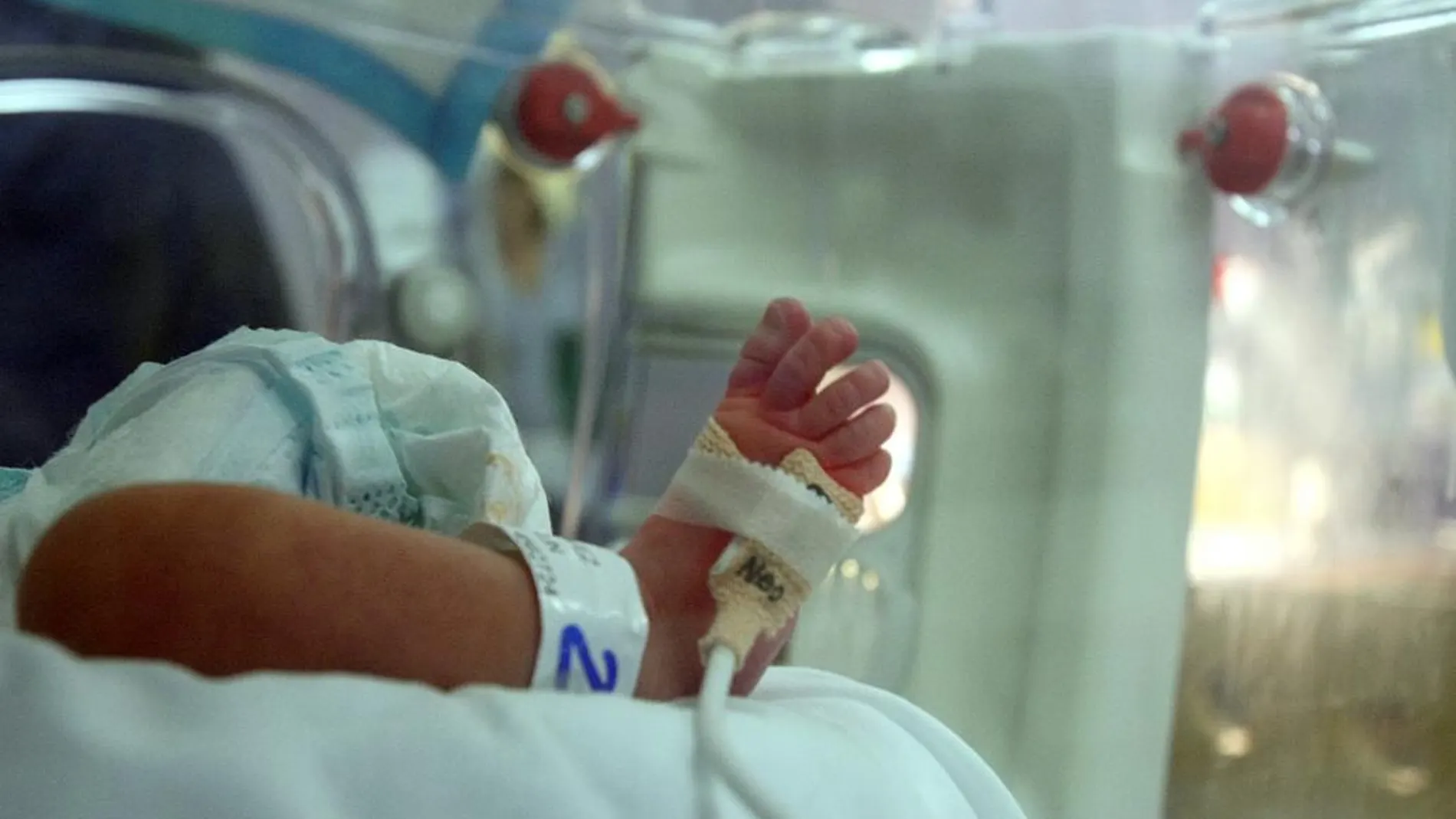
El ser humano necesita proteínas, y éstas, una vez ingeridas, se transforman en amoníaco. Sí, amoníaco, una sustancia tóxica que nuestro cuerpo es capaz de metabolizar y convierte en urea que posteriormente es expulsada del organismo a través de la orina. Sin embargo, uno de cada 50.000 recién nacidos no puede cumplir con esta función «automática». Sufren lo que se conoce como trastorno del ciclo de la urea (TCU), y es el responsable de que, entre el 25 y el 50 por ciento de los pequeños muera incluso antes de recibir un diagnóstico.
Cribado
Vicente Rubio, profesor de investigación del Consejo Superior de Investigaciones Científicas en el Instituto de Biomedicina de Valencia, y miembro del Ciberer, explica que «el amoníaco se acumula hasta que provoca daños muy graves en el sistema nervioso central, que pueden desembocar en encefalopatías y hacer que el paciente entre coma».
Un motivo por el cual los especialistas trabajan para poder desarrollar un sistema de cribado neonatal (la prueba de talón en el recién nacido) que permita realizar una detección temprana y facilite así el acceso a un tratamiento en las primeras horas de vida de los pequeños, ya que «los casos más graves de TCU se suelen presentar durante los primeros días de vida. De hecho, el bebé puede nacer sano, y pasadas las 48 horas, entrar en una situación de sopor que termina en coma y si se prolonga, puede producir daño cerebral irreversible (retraso mental) y morir en apenas una semana», añade Rubio.
Sin embargo, a día de hoy la prueba de talón no siempre es suficiente «porque hay casos que son tan precoces que los resultados de la prueba llegan tarde, y a eso se suma que hay casos que son especialmente difíciles de cribar».
La otra opción es el trasplante de hígado, algo bastante difícil, ya que, pese a los buenos expertos, es un gran riesgo para el bebé. «Por eso se intenta hacer lo posible para que el niño sobreviva el mayor tiempo posible y le operen a una edad más avanzada».
Terapia celular
Ante semejante panorama, la comunidad médica quiere apostar por la terapia celular que, si bien se encuentra en fase experimental, Rubio explica que «se aprobará en breve. Consiste en inyectar a la entrada del hígado (cateterizar la vena que entra al hígado) hepatocitos (que han sido aislados y procesados a partir de hígados donantes), algunos de los cuales se adhieren al tejido hepático y sobreviven, y de esta forma la situación metabólica mejora. Por los indicios, parece que ayuda a ganar tiempo para que el paciente alcance una edad adecuada para realizar un trasplante. Los resultados son muy positivos», añade.
Un proyecto que llega de la mano de Cytonet, empresa de biotecnología que trabaja con centros de metabolismo y neonatales que utiliza células hepáticas humanas saludables y metabólicamente funcionales para tratar estos problemas. Michael J. Deissner, gerente de Cytonet (compañía internacional de biotecnología que desarrolla el proyecto destaca que «es primordial que las familias afectadas tengan a su disposición toda la información necesaria y de apoyo para lograr que se sientan más seguros a la hora de hacer frente a este trastorno, por eso hemos realizado campañas de información al respecto», apunta Deissner.
En la actualidad, la compañía está pendiente de la aprobación por parte de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) de su terapia de células hepáticas humanas para tratar los trastornos del ciclo de la urea en pacientes pediátricos.
✕
Accede a tu cuenta para comentar


