
Medicamentos
Sanidad ordena la retirada definitiva de estos 66 productos homeopáticos
La Agencia Española de Medicamentos y Productos Sanitarios (Aemps) ha ordenado la retirada definitiva del mercado de 66 productos homeopáticos
La Agencia Española de Medicamentos y Productos Sanitarios (Aemps) -dependiente del Ministerio de Sanidad- ha ordenado la retirada definitiva del mercado de 66 productos homeopáticos al no haber aportado la documentación correspondiente para su autorización.
El Ministerio está llevando desde hace meses un proceso de autorización y registro de los productos homeopáticos en España para lo que estableció un calendario con plazos para que los fabricantes presentaran la documentación necesaria para su evaluación, según recuerda la Aemps en un comunicado.
Los 66 productos retirados que tienen indicación terapéutica o con vía de administración inyectable no han presentado la documentación requerida, por lo que la Aemps ha procedido a ordenar su retirada del mercado.
Estos son los productos retirados:
Aesculus-Injeel
Allium cepa Tendo compositum
Apis-Homaccord
Argentum metallicum D6
Berberis-Homaccord
Bronches/ Pyrite compositum
Cantharis Compositum
Cartílago Suis-Injeel
Cerusite D8
Chrysolithe compositum
Colocynthis-homaccord
Cor suis compositum n s
Cutis suis-injeel
Cynara scolymus-injeel
Disques vertebraux, Gelsemium
compositum
Dr- Reckeweg R16 Inject
Dr- Reckeweg R25 Inject
Dr. Reckeweg R10 Inject
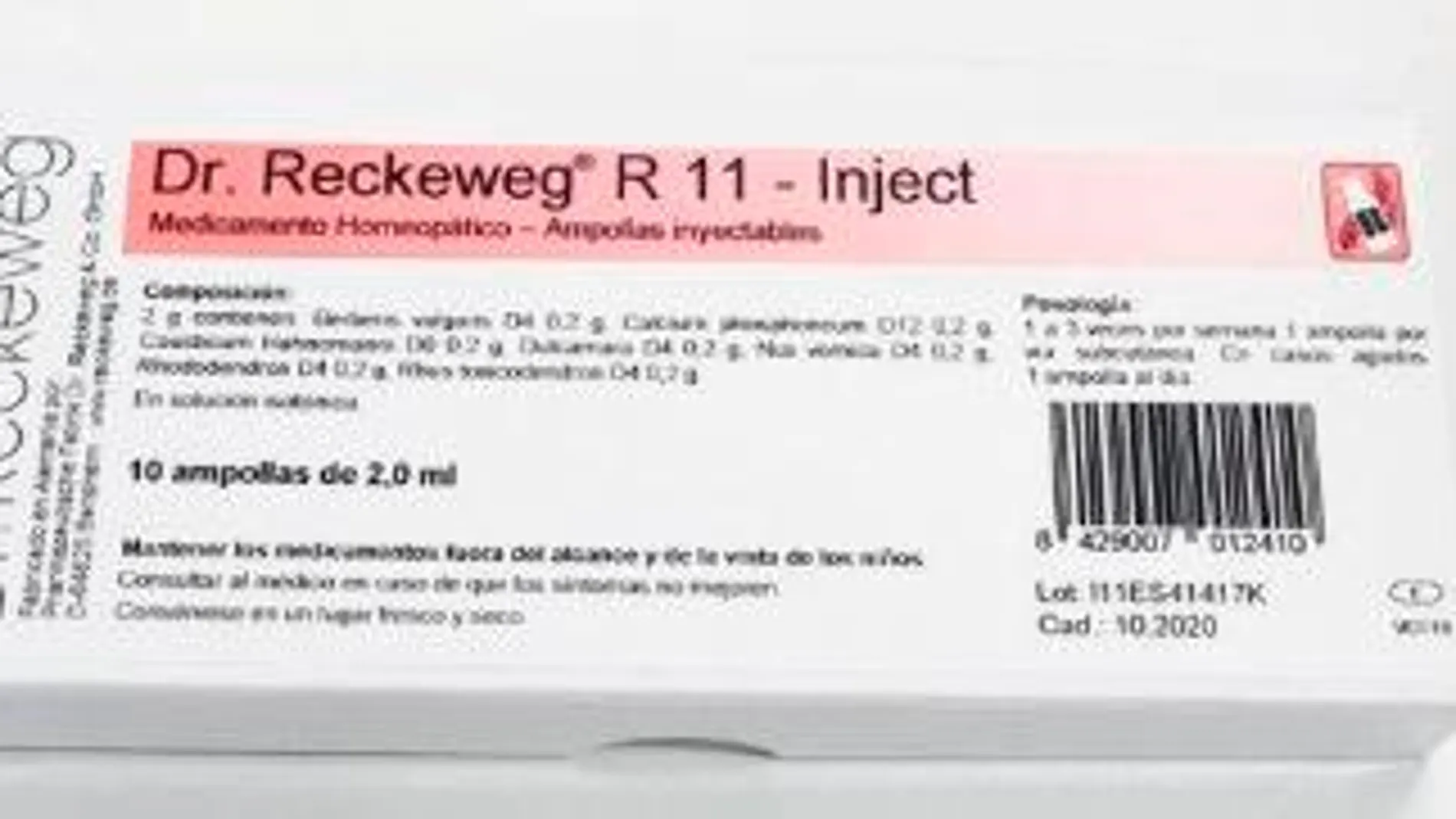
Dr. Reckeweg R11 Inject
Dr. Reckeweg R12 Inject
Dr. Reckeweg R17 Inject
Dr. Reckeweg R18 Inject
Dr. Reckeweg R2 Inject
Dr. Reckeweg R21 Inject
Dr. Reckeweg R34 Inject
Dr. Reckeweg R41 forte Inject
Dr. Reckeweg R41 Inject
Dr. Reckeweg R46 Inject
Dr. Reckeweg R49 Inject
Dr. Reckeweg R5 Inject
Dr. Reckeweg R54 Inject
Dr. Reckeweg R6 Inject
Dr. Reckeweg R63 Inject
Dr. Reckeweg R71 Inject
Dr. Reckeweg R73 Inject
Embryo Totalis suis-injeel
Ferrum Sidereum D20
Ferrum Sidereum, Phosphorus,
Silicea
Ferrum-Homaccord
Galium-Heel N
Gelsemium-Homaccord
Hamamelis-Homaccord
Hepar suis-injeel
Hepeel N
Hormeel SN
Hypophysis suis-injeel
Lamina Retina compositum
Mercurius Vivus D8
Metro-Adnex-Injeel
Neuro-injeel
Nux vomica-homaccord
Oscilogrip
Pankreas suis-injeel
Pfl arnicin
Pfl formiton
Pfl hepacel
Pfl sarcolax
Pfl uretene
Pfl venocel
Pulsatilla compositum
Ren suis-injeel
Scorodite D30
Silicea-injeel
Thuja-injeel
Tonico-injeel
Tonsilla Compositum n
Este organismo de Sanidad anunció el pasado 30 de abril la publicación de la orden ministerial que determinaba los requisitos mínimos y el procedimiento para que los productos homeopáticos se adecuaran al registro como estaba previsto en una directiva europea.
El pasado mes de octubre un total de 2.008 medicamentos homeopáticos pidieron a Sanidad adecuarse a la nueva regulación, mientras que el resto de productos que no cursaron su autorización dejaron de ser comercializados y fueron retirados del mercado.
La Aemps subraya en el comunicado que esos más de dos mil medicamentos que estaban a la venta no son productos autorizados por este organismo sino que se permite su comercialización hasta que se produzca la evaluación.
De esos 2.008, 66 son, por el momento, los productos denegados con lo que tendrán que abandonar el mercado.
Entre ellos se encuentran algunos como Berberis-Moaccord -para procesos inflamatorios del tracto urinario- Dr.Reckeweg R10 -para los síntomas de la menopausia-; Dr.Reckweg R11 Inject -para dolores musculares-; Oscilogrip -para los estados gripales y resfriados-; Pulsatilla Compositum -para estimular las defensas-; o Cartilago Suis Injeel- para dolores en el cartílago-, entre otros.
El calendario establecido por la Aemps consta de seis ciclos: el primero comprende la solicitud de los expedientes con indicación terapéutica (serán evaluados como el resto de los medicamentos siguiendo los mismos principios científicos) y aquellos sin indicación terapéutica cuya vía de administración sea inyectable.
Los productos del segundo ciclo en adelante son aquellos que se han notificado como 'sin indicación terapéutica' (con excepción de los inyectables) y que pueden acogerse al procedimiento de registro simplificado de acuerdo a la normativa.
Al finalizar la evaluación será cuando se determinen las condiciones de prescripción de este tipo de productos y será cuando deban incluir en el cartonaje y prospecto las leyendas que permitan la correcta identificación de los mismos.
Efe
✕
Accede a tu cuenta para comentar


