
Estados Unidos
Las «naves mensajeras» que crean metástasis
Los investigadores han conseguido “engañar” al tumor y colonizar el órgano que ellos habrían fijado.. Es una vía clave para desarrollar nuevos fármacos para bloquer las proteínas responsables
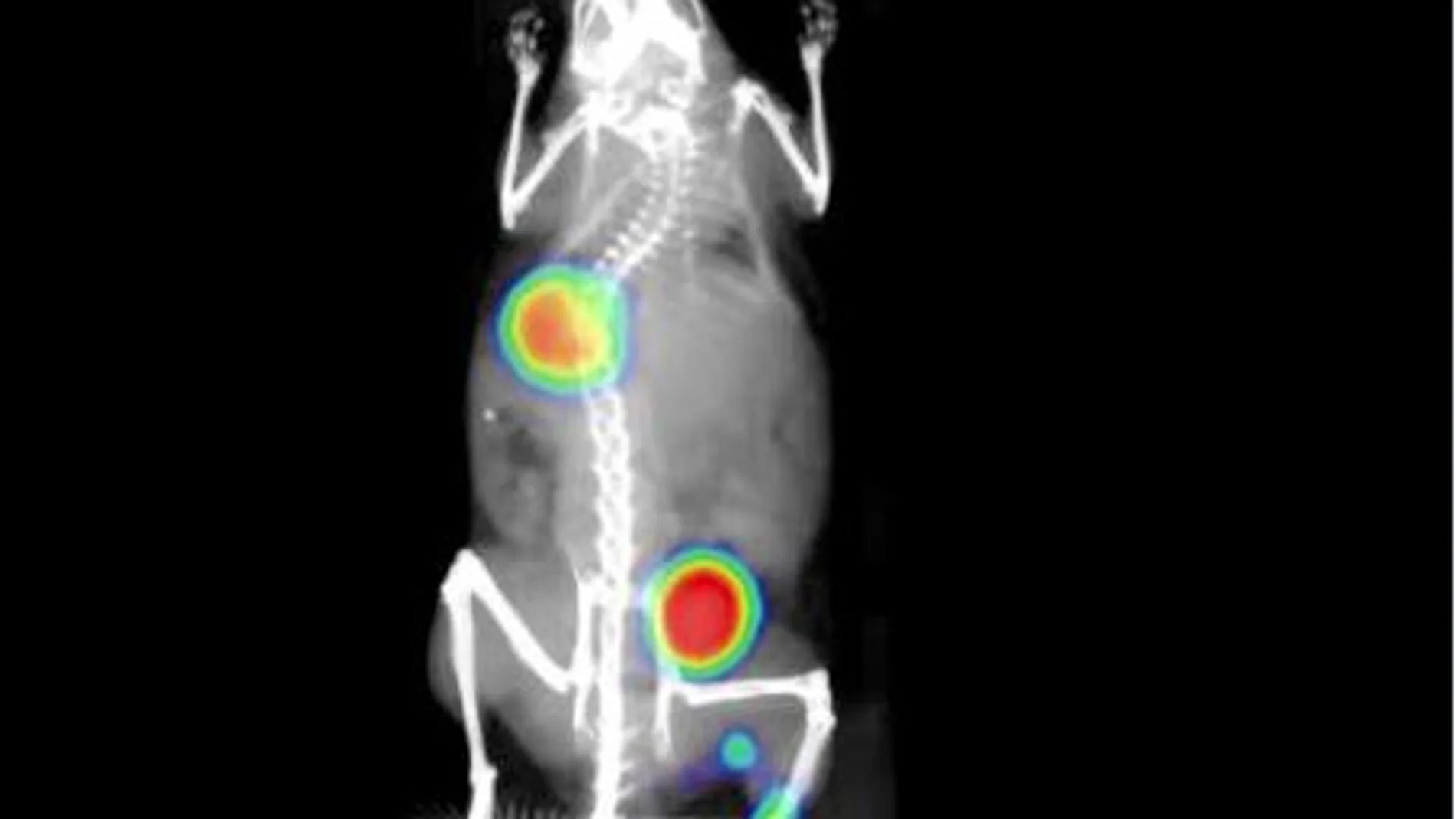
Los investigadores han conseguido “engañar” al tumor y colonizar el órgano que ellos habrían fijado. Es una vía clave para desarrollar nuevos fármacos para bloquer las proteínas responsables
Hace algo más de un siglo, el médico británico Stephen Paget planteó una teoría sobre la metástasis basada en la semilla y el sustrato. Paget defendía que la metástasis necesita células tumorales -semillas- que se dispersan en busca de un ambiente acogedor -sustrato fértil- en el órgano de destino.
Pero, hasta ahora, no se había conseguido identificar. Ciencuenta científicos de siete países diferentes, coliderados por un grupo español del Centro Nacional de Investigaciones Oncológicas (CNIO), el Weill Cornell Mediacl College y el Memorial Sloan Kettering Cancer Center, los dos de Estados Unidos han ido un paso más allá. Han descubierto que los tumores primarios envían “sondas mensajeras” capaces de transformar el ambiente en los órganos metastásicos, de forma que se vuelva acogedor para las células tumorales. Además, estos “destacamentos” del tumor llevan distintas “etiquetas moleculares” que funcionan como un código postal y les permite anidar en órganos específicos. “Este mecanismo que postulamos era hasta ahora desconocido en la formación de nichos metastásicos”, explica Héctor Peiinado, jefe del Grupo de Microambiente y metástasis del CNIO y uno de los participantes en el estudio.
La investigación, que se publica mañana en “Nature”, han hallado indicios de que los tumores emiten millones de vesículas cargadas con una representación de sus proteínas y de su material genético. Son los llamados exosomas, que funcionan como “naves mensajeras”. Son los responsables de que de que los órganos de destino estén preparados para acoger las células tumorales. Y es que son éstos los que desencadenan la respuesta molecular necesaria -inflamación y vascularización, entre otros- para acoger las células tumorales para que cuando lleguen puedan proliferar.
Durante estos tres años de investigación durante los que no sólo se ha trabajado con el modelo animal -células tumorales de ratón-, si no también con plasma de pacientes con cáncer, los investigadores escogieron varias líneas celulares de una decena de tumores distintos y de los que se sabe que algunos metastatizan a órganos concretos (pulmón, hígado, cerebro o hueso) y analizaron las proteínas de sus exosomas (cerca de un millar) en busca de las que podrían cumplir esa función de código postal. Se centraron en un grupo llamado “integrinas” porque se ubica en la membrana de los exosomas (las naves mensajeras) y allí descubrieron la “etiqueta”. “Hemos determinado que existe una combinación de integrinas en los exosomas tumorales que predispone la formación de nichos metastásicos en órganos concretos, específicamente en pulmón e hígado”, subraya Peinado. Si se engaña a un tumor cambiándole el “código de destino” podría colonizar el órgano que le indiquen. Y así lo probaron los científicos con células tumorales que normalmente irían al hueso y que consiguieron redirigir al pulmón.
Otra de las evidencias que han determinado en este estudio es que si se bloquean integrinas específicas en tumores que metastatizan a órganos concretos –por ejemplo cáncer de mama a pulmón y cáncer de páncreas a hígado–, se reduce la metástasis en esos órganos. Gracias a este descubirmiento se podrían detectar nuevas dianas “anti metástasis”. “Aún nos queda desarrollar test predictivos y validar nuestro estudio en grupos mayores, pero en el futuro nos planteamos crear fármacos para bloquear las combinaciones de integrinas específicamente en el tejido tumoral”, añade el investigador español.
✕
Accede a tu cuenta para comentar


