
Nueva York
La guindilla nueva arma contra el dolor neuropático
Un parche cutáneo, cuyo principio activo es un componente de los pimientos picantes, es capaz de sumir en un profundo sueño a las terminaciones nerviosas dañadas y proporcionar calidad de vida a los pacientes. Así quedó reflejado en el XIII Congreso Internacional sobre Dolor
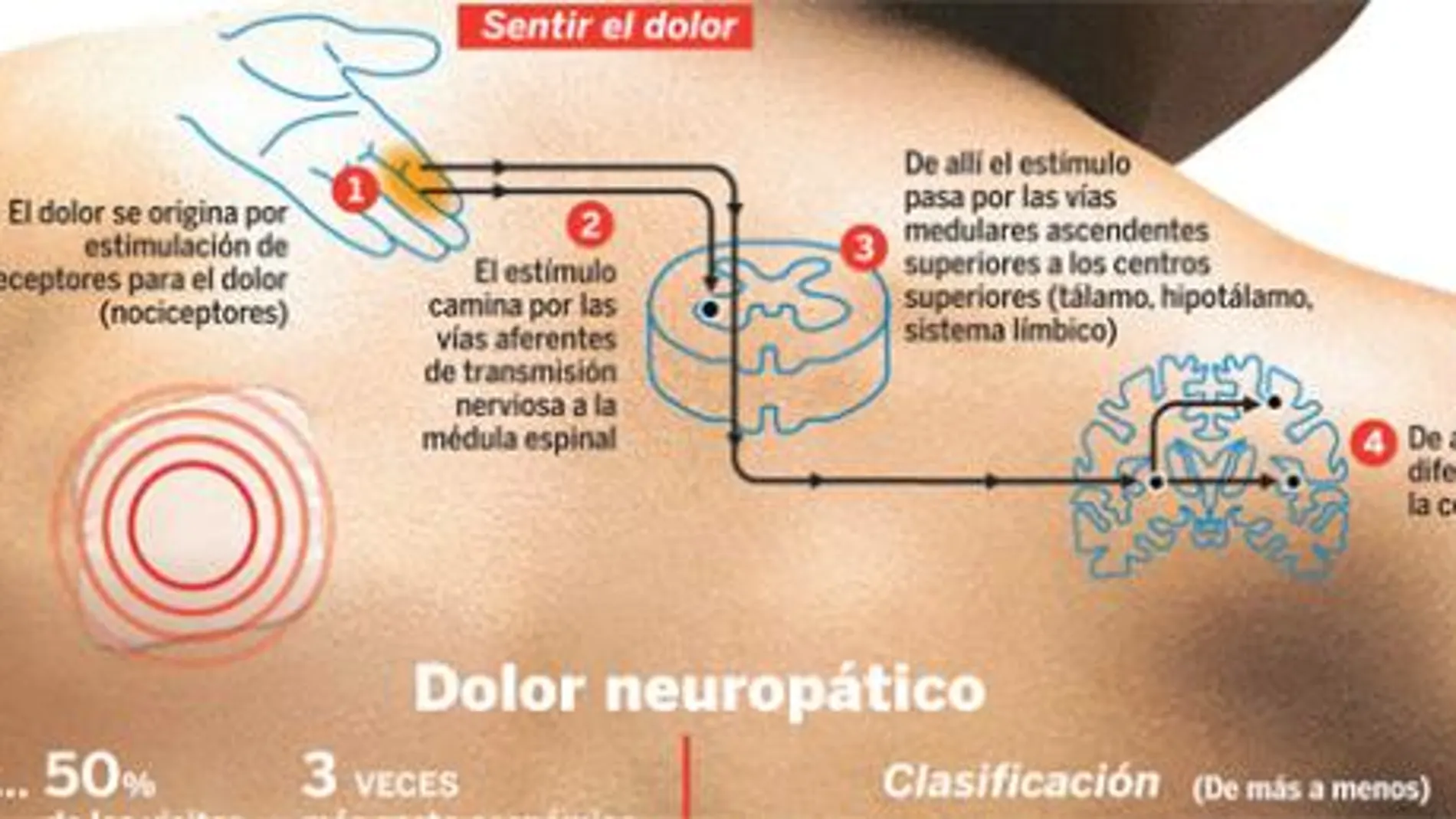
Punzante, ardiente, constante y continuo hormigueo son, entre otras, las palabras con las que los pacientes describen el tormento con el que conviven día a día. Entre un tres y ocho por ciento de los europeos sufre dolor neuropático, en España cerca de tres millones de personas. Un síndrome que conlleva importantes desajustes emocionales ante la impotencia de ver cómo su vida se desmorona por culpa de una alteración del sistema nervioso. Esta lesión orgánica se debe, sin embargo, a una respuesta inadecuada del cuerpo ante un estímulo tan leve, como por ejemplo el simple roce de la ropa, tal como explica Rolf-Detlef Treede, del Centro de Biomedicina y Tecnología Médica de Manheim de la Universidad de Heidelberg (Alemania). «Este daño en muchas ocasiones pasa desapercibido y se encuentra infradiagnosticado. Por ello, los enfermos sufren los consecuencias que minan su calidad de vida y desarrollan crisis depresivas», apunta Treede, que además pertenece a la Asociación Internacional para el Estudio del Dolor (IASP, por sus siglas en inglés).
Un halo de esperanza
En la última reunión de esta sociedad médica, celebrada la semana pasada en Montreal, se presentó uno de los últimos y más prometedores avances para esta patología. Un parche cutáneo que asegura 12 semanas de alivio del dolor neuropático periférico, consecuencia directa de algunas lesiones de espalda, neuropatía diabéticas dolorosas, las asociadas al virus del sida y la postherpética. David Simpson, profesor de Neurología de la Facultad de Medicina del Mount Sinai de Nueva York (EE UU), explica que «el objetivo del tratamiento no es sólo aliviar el dolor para mejorar el estado del paciente y ayudar a los enfermos a recuperar sus actividades diarias. Los nuevos datos recogidos de los últimos estudios sugieren que la elevada concentración de capsaicina en el parche tiene el potencial suficiente para manejar satisfactoriamente la dolencia».
Esta optimista perspectiva se debe a que más de un 50 por ciento de los pacientes responde correctamente a los efectos del parche, ya que ve disminuido el dolor del todo, o casi, al menos durante doce semanas. ¿Dónde está la clave? Luis Aliaga Font, jefe de la Clínica del Dolor del Centro Médico Teknon de Barcelona, asegura que «esto se debe a la elevada concentración de capsaicina –hasta un ocho por ciento–, que en otros fármacos tópicos no supera el uno por ciento».
Pero, ¿qué es la capsaicina? Es el componente activo de los pimientos picantes, como el chile o la guindilla. Resulta interesante cómo esta sustancia, responsable de provocar el picor y el ardor en la boca tras el primer mordisco, tiene la capacidad suficiente para calmar la misma sensación en el organismo. Una forma de estimular el «sueño» o adormecer los nervios dañados durante un tiempo y evitar las incomodidades al enfermo.
Dadas las evidencias probadas de este medicamento –comercializado como Qutenza, por el laboratorio japonés Astellas Pharma–, que han visto la luz en prestigiosas revistas científicas como «Nature», las agencias reguladoras de la aprobación de nuevos fármacos europea y americana –EMEA y FDA, respectivamente– ya le dieron luz verde para que los pacientes más necesitados puedan tratarse con el parche dérmico. Pese a que ya está disponible en países europeos, como Alemania, Austria y Reino Unido, en España aún tardará algunos meses ya que está pendiente de las negociaciones de precio y reembolso. Aunque, como apunta Aliaga, puede que existan casos de uso compasivo, «si los pacientes que no responden a los otros tratamientos prefieren probar una alternativa menos drástica a las terapias invasivas –quirúrgicas–, se puede solicitar al Ministerio».
«¿Puedo usar el parche?»
Antes de nada el paciente ha de estar diagnosticado de la enfermedad en concreto. Burkhard Gustorff, jefe del Departamento de Anestesiología y Cuidados Intensivos Médicos del Hospital Kaiserin Elisabeth de Viena (Austria), especifica que «el parche está indicado en el tratamiento del dolor neuropático periférico en adultos no diabéticos, sobre todo en los que proceden de lesiones herpéticas y asociadas al VIH –virus de inmunodeficiencia humana–».
Puede haber muchos tipos de dolor neuropático, pero tiene que haber una enfermedad que lo provoque. Aliaga establece que se deben de cumplirse al menos tres de cuatro criterios establecidos, «como son: que el enfermo tenga una distribución anatómica consecuente con los principios tipográficos de diagnóstico de neurología; que el daño producido tenga una historia sugestiva de lesión; que haya alguna exploración que concuerde –como electromiografía, resonancia...–; y que las dos primeras coincidan».
En el caso del dolor que procede de la neuropatía postherpética, «la sensación de quemazón, hormigueo y calambre que caracteriza a este tipo de dolor dura más de 36 meses en el 43 por ciento de los pacientes», según manifiesta Ralf Baron, del Departamento de Neurología de la Universidad Christian Albretchs, en Kiel (Alemania).
Una vez comprobado que el enfermo se encuentra apto para recibir el tratamiento, se procede a la colocación del parche. Esto se lleva a acabo en un hospital, donde se pueden observar las reacciones adversas del mismo, que en este casos son muy pocas y en su mayoría se hallan a nivel cutáneo, como reacciones dérmicas. «Primero se pinta la zona donde el paciente experimenta el dolor y se aplica un gel anestésico, luego se procede a la colocación del parche, que debe permanecer pegado a la piel de treinta minutos a una hora, según sea el área corporal», detalla Simpson. Carlos Barutell, jefe de la Clínica del Dolor del Hospital Vall de Hebron de Barcelona, se muestra cauteloso y puntualiza que «la elevada concentración de la capsaicina puede ser muy argesiva para algunos pacientes. En ellos en vez de aplicar un analgésico previo, hay que emplear morfina y la piel queda totalmente roja».
Con este sistema, los pacientes cumplen al cien por cien con la terapia, al mismo tiempo que los médicos pueden saber con toda certeza si el fármaco funciona como se espera. «Los pacientes que he podido tratar han experimentado una notable mejoría. Cuentan que pueden llevar una vida normal, salir a la calle, hacer la compra... para muchos ha significado recuperar su independencia y su vida social», argumenta Gustorff. Tras la aplicación, los primeros efectos se observan en las 24 a 48 horas siguientes. «En el caso de que el alivio sólo sea parcial, no hay inconveniente para administrar otros analgésicos de forma conjunta, ya que no presenta interacciones», añade Gustorff.
Una de las cuestiones que se planteó durante la presentación en el congreso era la posible continuidad del tratamiento tras las doce semanas que se establecían en los estudios. Los expertos aseguraron que se puede emplear de forma indefinida, «ya que se ha de mostrado que el uso continuado reduce la zona a tratar poco a poco sin tener que elevar las dosis, e incluso, al contrario, quizás se disminuyan», apunta Simpsom.
De esta forma, los pacientes tienen acceso a una terapia menos tóxica, pero más eficaz, que no necesita de una continua suma de dosis cada vez que el enfermo nota que la medicación pierde fuerza.
cannabis, a debate
Otras de las alternativas al tratamiento de dolor crónico es el uso del cannabis, sobre todo si su forma de administración es oral, es decir, de forma inhalada, a modo de cigarrillo. Fernando Cerveró, presidente electo de la IASP y jefe de la Unidad de Investigación de Anestesia de la Universidad de McGill en Montreal, Canadá, explica que «esto se debe a los problemas que puede presentar de cara a la sociedad el plantear este tipo de terapias, que ya han demostrado su utilidad en algunos campos como en el dolor crónico y canceroso».
Aunque también señala los efectos secundarios, como la adicción. «En pacientes con expectativas de vida larga creo deben emplearse cuando todos los otros tratamiento han fracasado y teniendo un seguimiento muy estricto para evitar efectos indeseables y problemática de mal uso y abuso que tan grave problema está causando en otros países, sobre todo EEUU y que en el nuestro aunque de momento no se presenta debemos estar prevenidos para evitarlos. No debemos emplearlos "alegremente"como ultimamente estamos observando», manifiesta Barutell.
Uno de los estudios presentados durante las sesiones plenarias del congreso hacía referencia a este aspecto. Para la población que sufre dolor crónico, fumar cannabis reduce el dolor, mejora el humor y ayuda a conciliar el sueño, según publicaba «Canadian Medical Association Journal», durante la cita internacional. El trabajo, realizado por un equipo de investigadores de la Universidad de McGill, explica los beneficios de tomar así el fármaco.
«Hemos encontrado que con 25 mg de esta sustancia, con un 9,4 por ciento del tetrahidrocannabinol (THC), administrado en una sola inhalación tres veces al día durante cinco, reducimos perceptiblemente la intensidad media del dolor comparada con un placebo en adultos con dolor crónico neuropático posquirúrgico», explica Mark Ware, autor de los informes de la investigación clínica en la unidad de gerencia del dolor Alan Edwards del Centro médico Universitario de McGill. «Además, descubrimos que hay significativas mejoras a través de las medidas de la calidad del sueño y de los episodios de ansiedad», añade Ware. Desde la Universidad de Oxford, en Reino Unido, Henry McQuay, de la Facultad de Balliol, plantea que la investigación ayuda a dar respuestas terapéuticas a los pacientes que están pasando una auténtica pesadilla y que ven que este tipo de sustancia puede servir de alivio a su tormento.
Nuevas vías de estudio
Puesto que el dolor tiene su origen en una lesión nerviosa que se manifiesta a nivel cerebral, el futuro de la especialidad que la trata pasa por encontrar las claves para entender los mecanismos concretos de acción.
«Queremos saber cómo se desarrollan los procesos de cronificación del dolor», explica Cerveró, que asegura que la neurociencia cerebral podrá dar respuestas a estas incógnitas. «Conocer el desarrollo neuronal podrá servir para encontrar nuevas dianas contra las que podrían actuar los medicamentos que descubramos en el futuro». En este sentido, los investigadores buscan mediadores moleculares que intervengan en la maquinaria cerebral que transmite las señales de la percepción del dolor. El presidente electo de la IASP confía en que esta especialidad dé muchas respuestas clave en el tratamiento del dolor y le augura un futuro prometedor. En este campo, se desarrollaron algunas ponencias que apuntaban a ciertos mecanismos, aún en una fase muy inicial de estudio.
Cerveró, también apunta a la importancia de la sinergia entre Atención Primaria y las diferentes especialidades y las Unidades del Dolor con el fin de beneficiar a los pacientes que tiene dificultades de acceso a los tratamientos, bien por encontrarse en zonas de dificil acceso o en países en vías de desarrollo en las que las oportunidades de recibir ayuda son casi nulas.
Entender el dolor en los neonatos
Durante el XXII congreso de la asociación internacional para el estudio del dolor, celebrado en Montreal, se presentaron algunas claves para abordar este aspecto en los bebés
Celeste Johnston, profesora de Enfermería de la Universidad McGill de Montreal (Canadá) y presidenta de la Coalición Canadiense del Dolor, ofreció en una de las sesiones plenarias un análisis del abordaje terapéutico y el manejo del dolor en los más pequeños. Bajo el título «Desde la boca de los bebés: qué hemos aprendido de las investigaciones sobre dolor en neonatos», Johnston desgranó los avances más significativos en cuanto a control del dolor, desde el punto de vista no farmacológico, «con el fin de evitar grandes daños en los bebés y que éstos tengan que sufrir las consecuencias en la edad adulta».
Durante las pasadas dos décadas, el volumen de investigaciones sobre este síndrome en los recién nacidos ha experimentado un crecimiento considerable. En la actualidad, existen claras evidencias de que los neonatos no son ni mucho menos respondedores pasivos al dolor ni a las terapias analgésicas intervencionistas. La respuesta de los neonatos al dolor agudo se puede medir y difieren de las que se van dando a través de los diferentes tipos de abordaje terapéutico (analgésicos, opiáceos...). Los nuevos enfoques para medir el nivel del dolor han proporcionado validez científica a ciertos métodos observacionales. «En muchos casos, centrarse en el cambio de las expresiones faciales de los pequeños resulta una pieza clave para saber si funciona o no la terapia», apunta Johnston.
La edad de desarrollo así como la exposición anterior del dolor es determinante ante la respuesta que pueda experimentar el bebé, así como consecuencias a largo plazo, es decir, en la edad adulta, «casi todos se ven entre los nueve y catorce años, en el modo en que se enfrentan a este tipo de experiencias clínicas», añade Johnston. Los cambios considerados debido a la exposición repetida al dolor en el recién nacido rápidamente pueden convertirse en profundos.
Los anestésicos tópicos y las intervenciones no farmacológicas se han probado de forma intensiva en recién nacidos, dado que el uso extendido de terapias a base de medicamentos estándar resulta problemático en el recién nacido. Johnston subraya la eficacia significativa de los tratamientos no farmacológicos, en concreto el uso de la sacarosa y la terapia piel con piel o método canguro, en el que el bebé siente alivio continuado.
✕
Accede a tu cuenta para comentar


