
Salud
Combatir la resistencia a los fármacos, un desafío global
Un equipo de científicos ha descubierto cómo las bacterias esquivan a los antibióticos
La resistencia a los antimicrobianos (AMR, por sus siglas en inglés) se produce cuando las bacterias, los virus, los hongos y los parásitos ya no responden a los medicamentos, lo que hace que las infecciones sean más difíciles de tratar y aumente el riesgo de propagación de patologías, enfermedades graves y muerte.
De acuerdo con la Organización Mundial de la Salud (OMS), se trata de uno de los problemas más importantes a los que se enfrenta la sanidad mundial. A partir del año 2050 se cobrará la vida de 10 millones de personas anualmente y su coste en la economía global será altísimo si no logramos cambiar los pronósticos.
Recientemente, un equipo de científicos australianos, liderados por Timothy Barnett, ha descubierto una nueva forma de resistencia a los antimicrobianos que era indetectable mediante los métodos de prueba de laboratorio tradicionales. Básicamente, se trata de cómo las bacterias logran esquivar los antibióticos.
El equipo de Barnett realizó el hallazgo, publicado en «Nature Communications», mientras investigaba la susceptibilidad a los antibióticos del estreptococo del grupo A, una bacteria potencialmente mortal que a menudo se encuentra en la garganta y en la piel y de reciente actualidad por las infecciones que está provocando en países como Reino Unido, Francia o, incluso, España.
«Las bacterias necesitan producir sus propios folatos (ácido fólico, importante en la formación de los glóbulos rojos y para el crecimiento y la función saludables de las células) para crecer y, a su vez, causar enfermedades. Algunos antibióticos funcionan al bloquear esta producción de folato para detener el crecimiento de bacterias y tratar la infección –explica Barnett en un comunicado del Instituto Telethon–. Al observar un antibiótico comúnmente recetado para tratar las infecciones de la piel por estreptococos del grupo A, encontramos un mecanismo de resistencia en el que, por primera vez, la bacteria demostró la capacidad de tomar folatos directamente de su huésped humano cuando se les impedía producir los suyos propios. Esto hace que el antibiótico sea ineficaz y es probable que la infección empeore cuando el paciente debería estar mejorando. Esta nueva forma de resistencia es indetectable con los métodos habituales, lo que hace que sea muy difícil recetar antibióticos que traten eficazmente la infección, lo que podría conducir a resultados muy deficientes e incluso a la muerte prematura».
Esto demuestra, como explica Barnett, que comprender los mecanismos de AMR es mucho más complejo de lo que se pensaba y se necesitará aún más investigación. Y aquí hace su entrada otro estudio publicado por científicos de la Universidad Tecnológica de Dinamarca (DTU).
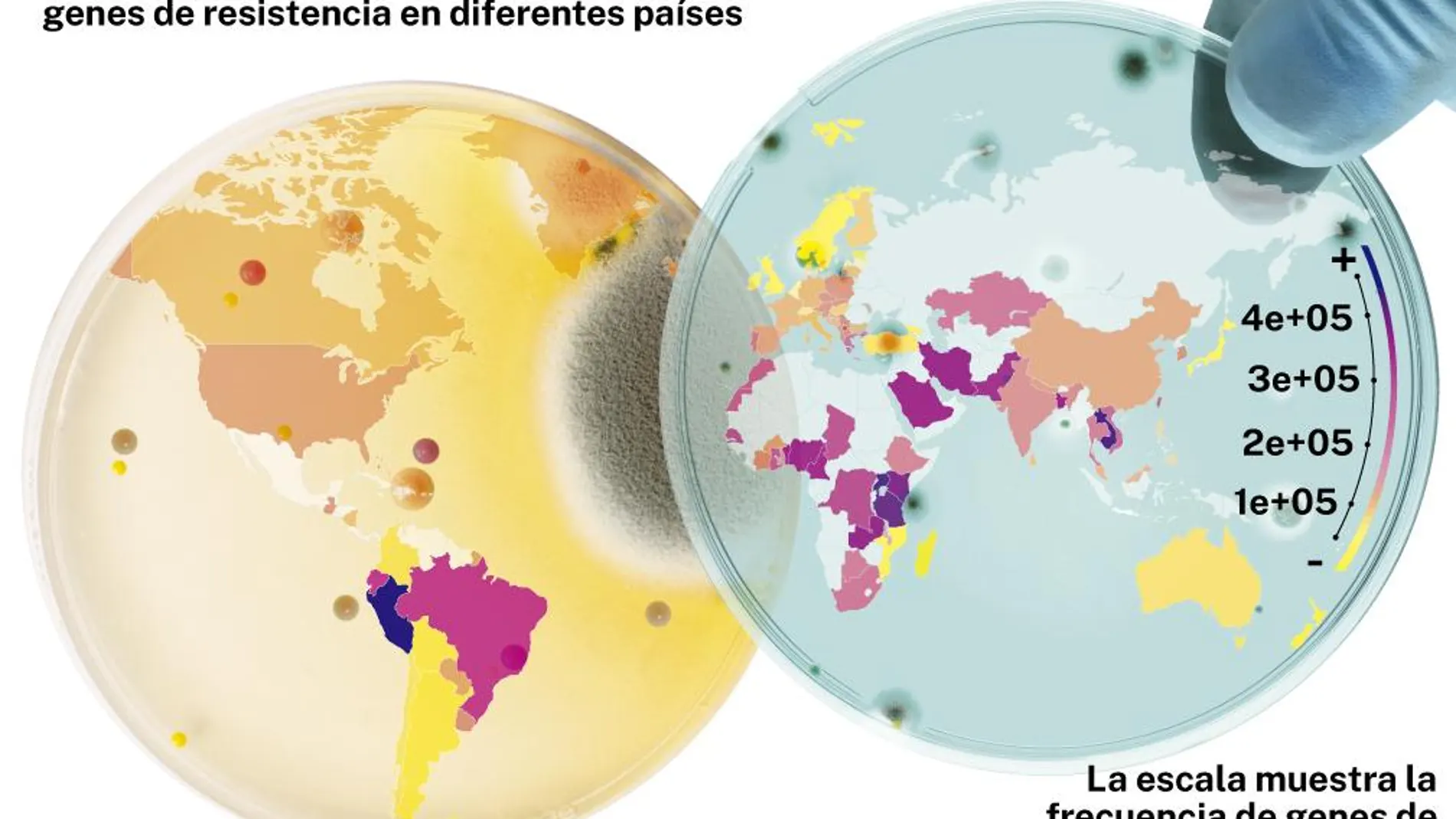
Durante la pandemia de Covid-19, los expertos se han dado cuenta del valor de usar análisis de aguas residuales para monitorizar el desarrollo de enfermedades en un área. Al analizar los desechos de una población se descubren las bacterias más frecuentes en la región y si tienen o no algún tipo de resistencia a los antibióticos. El Instituto Nacional de Alimentos de la DTU lleva más de un lustro utilizando esta herramienta efectiva y económica para analizar enfermedades infecciosas y resistencia a los antimicrobianos. Y ahora han presentado un mapa global de la resistencia antimicrobiana.
Mediante el análisis de muestras de aguas residuales de 243 ciudades en 101 países entre 2016 y 2019, un equipo liderado por Patrick Munk ha elaborado un mapa que muestra los países en los que aparecen los genes que dotan de esta resistencia a los microbios. En total, se analizaron 757 muestras de aguas residuales. La ventaja de este sistema, que contempla el análisis genómico de las aguas residuales, es que es un método rápido y bastante económico en relación con la cantidad de personas que puede cubrir. Tampoco precisan de la aprobación por parte de un comité de ética, ya que el material de muestra no puede vincularse a individuos.
Ambas herramientas sirven para profundizar en nuestro conocimiento sobre la resistencia de los microbios y evitar que estos se propaguen.
«AMR es una pandemia silenciosa de mucho mayor riesgo para la sociedad que la de Covid-19 –añade Barnett–. Además de 10 millones de muertes por año para 2050, la OMS estima que le costará a la economía mundial unos 100 billones de euros si no podemos encontrar una manera de combatirla. Sin antibióticos, nos enfrentamos a un mundo en el que no habrá forma de detener las diferentes infecciones mortales, los pacientes con cáncer no podrán recibir quimioterapia y las personas no tendrán acceso a cirugías. Para preservar la eficacia a largo plazo de los antibióticos necesitamos identificar y comprender mejor los nuevos mecanismos de resistencia a los antibióticos, lo que ayudará en el descubrimiento de nuevos antibióticos y nos permitirá controlar la AMR a medida que surja»
De cara al futuro, los expertos ya están centrados en desarrollar métodos de prueba para detectar este mecanismo de resistencia a los antibióticos para permitir un tratamiento eficaz.
«Es importante contar con nuevas herramientas de diagnóstico que puedan detectar rápidamente la resistencia a los antibióticos, incluida la resistencia dependiente del huésped –añade el coautor del estudio, Kalindu Rodrigo–. Es vital que nos mantengamos un paso por delante de los desafíos de la AMR. Por otro lado, se deben realizar esfuerzos iguales en todos los niveles de la sociedad, incluidos los pacientes, los profesionales de la salud y los encargados de formular políticas, para ayudar a reducir los impactos de la AMR».
✕
Accede a tu cuenta para comentar





