
Ministerio de Sanidad
Fabricar una vacuna requiere de dos años
Producir una dosis totalmente segura es un proceso largo y complejo. Por eso, en situaciones especiales de demanda, pueden darse problemas en el suministro
Producir una dosis totalmente segura es un proceso largo y complejo. Por eso, en situaciones especiales de demanda, pueden darse problemas en el suministro
Hace unos días saltaba la noticia de la vuelta a las farmacias de la vacuna de la meningitis B, tras meses sin dosis por problemas de desabastecimiento en toda España que se debió a retrasos en los lotes que estaban asignados para recibirse en enero. Apenas dos semanas antes, se retomaba también la administración de la dosis de recuerdo de la vacuna contra la tosferina para niños de seis años. En este caso el retraso fue debido a los problemas de suministro internacional, y ante el cual se priorizó inmunizar a las embarazadas para proteger así a los recién nacidos.
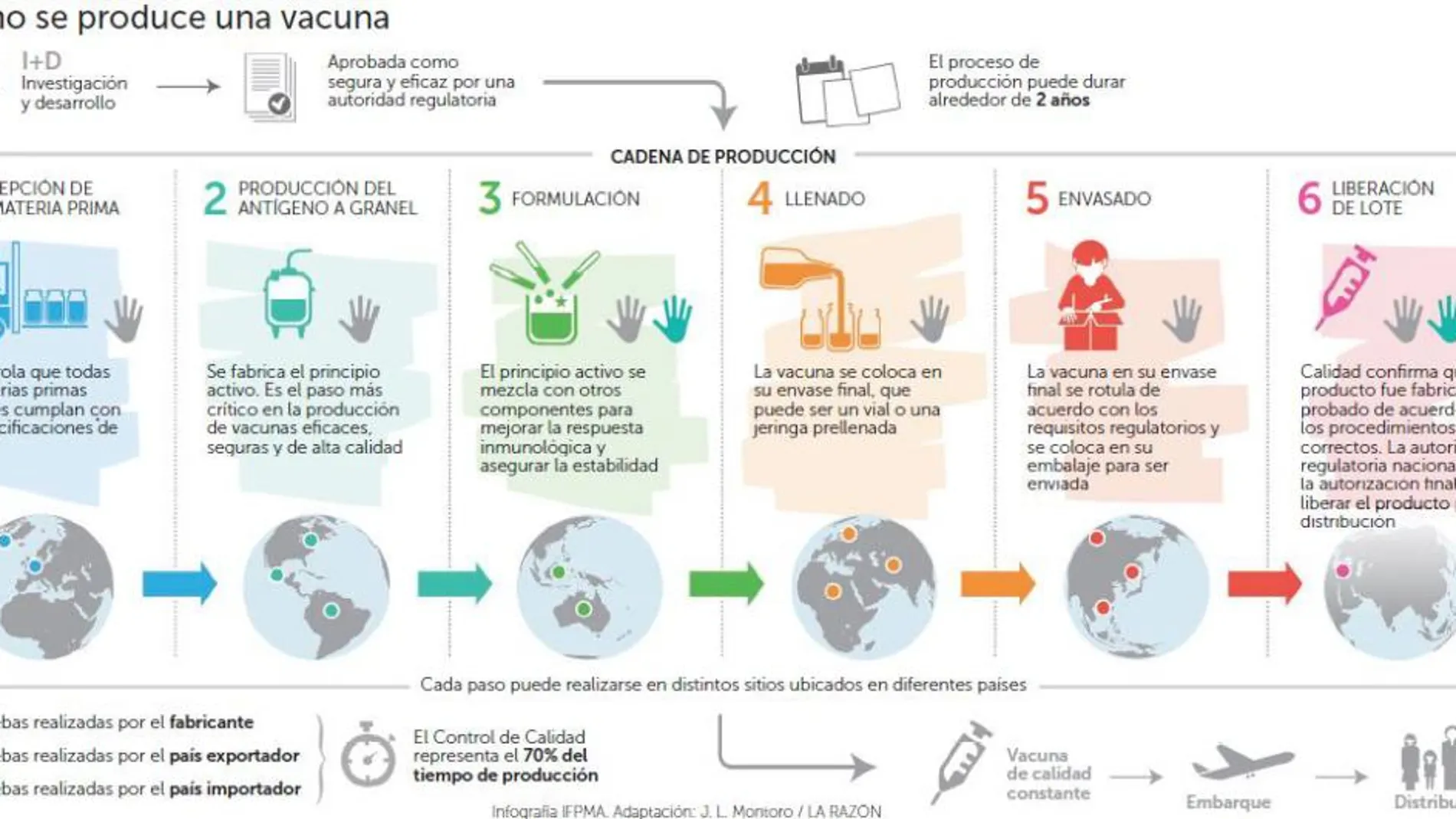
Ambas situaciones, que generaron cierta alarma social, se explican mejor si se conoce el complejo proceso que entraña la fabricación de una vacuna. No hablamos del trabajo de investigación y desarrollo de las mismas, sino de su «simple» producción. Y es que, como señala Clive Blatchford, vicepresidente de Calidad de Vacunas de la compañía farmacéutica GSK, «lo que se fabrica hoy, con las previsiones a día de hoy, no estará disponible hasta dentro de dos años». Así de complejo es el proceso y de largo el plazo de producción. (ver gráfico)
Todo ello puede comprometer la capacidad de responder con celeridad a la variabilidad de la demanda. Eso fue lo que pasó con la vacuna de la meningitis B (Bexero, por su nombre comercial, fabricada por GSK), que en España no está financiada por la Sanidad pública: «Se generó una gran demanda por diferentes motivos en todo el mundo, pero tardamos 24 meses en prepararla», asegura Blatchford.
Pese a ello, las medidas puestas en marcha para hacer frente a esa demanda pasaron, por una parte, por ampliar la producción y acelerar, en la medida de lo posible, los procesos. «Hemos introducido mejoras para producir un poco más. Hemos reducido los tiempos y mejorado los volúmenes y el rendimiento de las plantas, pero no podemos comprometer los procesos. No podemos liberar vacunas que no sean seguras», continúa. Por otra, en no abrir nuevos mercados «para poder cubrir la demanda en los ya presentes», apunta Francesca Ceddia, vicepresidente de Asuntos Médicos Globales Vacunas de GSK. La creación de una nueva planta de fabricación en Alemania se espera alivie también la presión, si bien hasta finales de 2019, principios de 2020 no estará activa.
El suministro y la demanda de vacunas es una cuestión de equilibrio: así, mientras la demanda aumenta globalmente y es variable en situaciones de crisis, el suministro tiene un número limitado de fabricantes y capacidad de producción mundial. «Intentamos anticiparnos para no recibir sorpresas. Hay convocatorias de proveedores de países. También hacemos predicciones de lo que vamos a necesitar y estas predicciones son bastante ajustadas, pero hay más necesidad que vacunas», lamenta Blatchford.
Seguridad ante todo
La fabricación de vacunas es un proceso largo y complejo en aras de la seguridad. Basten como ejemplo algunas cifras, como que el control de calidad representa el 70% del tiempo de producción, que los procesos de limpiado de los recipientes y materiales empleados duran entre 8 y 12 horas o que el protocolo de esterilización del personal para entrar a las instalaciones de trabajo requieren, estando entrenados, de 20 minutos.
La respuesta ante las crisis
Hay situaciones especiales, como ante una crisis sanitaria, en que los procesos de desarrollo de una vacuna puede determinar la vida o la muerte. Eso fue lo que pasó con la última del ébola en África.
«El primer caso se detecta en diciembre de 2013 y en agosto de 2014 se declara a epidemia. Es entonces cuando la empresa decide que quiere hacer algo. Vemos que hay una vacuna candidata y que los datos iniciales de los ensayos muestran que presenta un aceptable perfil de seguridad», explica Philippe Denoel, director R&D vacunas de GSK. «Tuvimos que producir a toda velocidad e invertir una gran cantidad del fondo de desarrollo de vacunas», continúa Denoel, en un trabajo de colaboración con diferentes organismos internacionales volcados en evitar que la epidemia se propagase. La vacuna, con resultados prometedores en macacos, se prueba contrarreloj, con ensayos de fase I para demostrar su seguridad en 200 voluntarios sanos y, en enero de 2015 está listo el primer lote, de viales, que sirve para arrancar un gran ensayo clínico que implica a más de 30.000 personas voluntarias.
✕
Accede a tu cuenta para comentar


