
Pandemia
Así es Evusheld, el medicamento de AstraZeneca que previene la covid y que fue autorizado por EE UU para los ‘antivax’
Una dosis de este fármaco contra el coronavirus puede ser eficaz para la prevención previa a la exposición durante seis meses
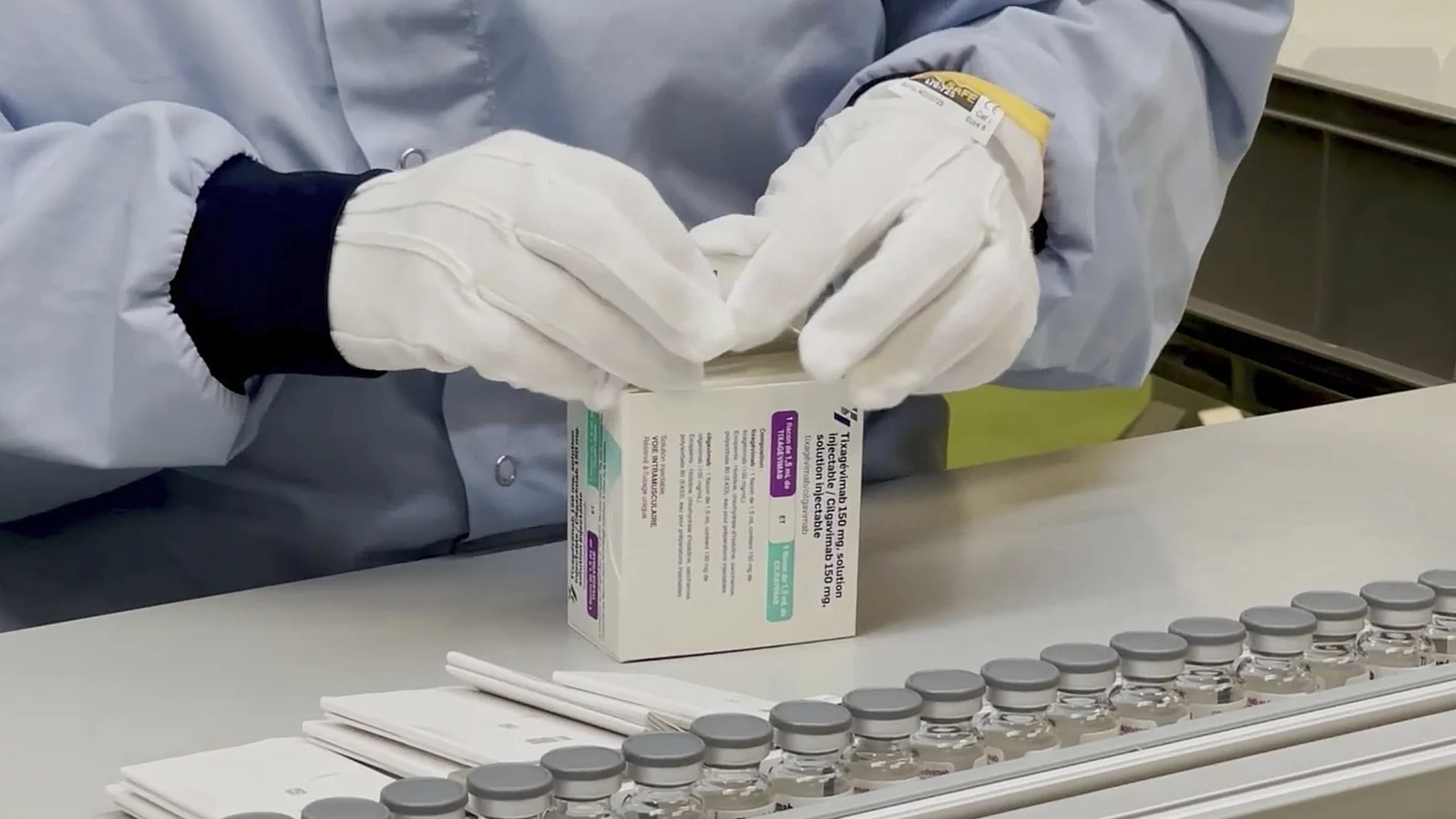
La Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) ha emitido una autorización de uso de emergencia para dos anticuerpos monoclonales que previenen la covid-19 y combinados en un solo fármaco, ‘Evusheld’, de AstraZeneca, para personas inmunodeprimidas o con alergias severas a las vacunas.
Este se compone de tixagevimab y cilgavimab, y, en concreto, está indicado para adultos y niños de 12 años de edad o más que pesen al menos 40 kilogramos y tengan un sistema inmunitario entre moderado y grave, debido a una afección médica o a la toma de medicamentos o tratamientos inmunosupresores y que no puedan dar una respuesta inmunitaria adecuada a la vacunación contra la covid-19.
Además, este fármaco también se destina a personas con un historial de reacciones adversas graves a una vacuna contra la covid-19 y/o a uno o varios de sus componentes, es decir, a personas a las que no se recomienda la vacunación, según el calendario aprobado o autorizado.
Asimismo, el producto solo está autorizado para aquellas personas que no estén actualmente infectadas por el virus del SARS-CoV-2 y que no hayan estado expuestas recientemente a una persona infectada por el SARS-CoV-2.
Precisamente, el tixagevimab y el cilgavimab son anticuerpos monoclonales de acción prolongada dirigidos específicamente contra la proteína de la espiga del SARS-CoV-2, diseñados para bloquear la adhesión y la entrada del virus en las células humanas. El tixagevimab y el cilgavimab se unen a sitios diferentes y no superpuestos de la proteína de la espiga del virus.
“Las vacunas han demostrado ser la mejor defensa disponible contra el coronavirus. Sin embargo, hay ciertos individuos inmunocomprometidos que pueden no montar una respuesta inmune adecuada a la vacunación contra la covid-19, o aquellos que tienen un historial de reacciones adversas graves a una vacuna contra la covid-19 y por lo tanto no pueden recibir una y necesitan una opción de prevención alternativa”, ha dicho la directora del Centro de Evaluación e Investigación de Medicamentos de la FDA Patrizia Cavazzoni.
“La acción de hoy autoriza el uso de la combinación de dos anticuerpos monoclonales para reducir el riesgo de desarrollar covid-19 en estas personas”, ha añadido.
Una dosis de ‘Evusheld’, administrada en dos inyecciones intramusculares separadas y consecutivas (una inyección por anticuerpo monoclonal, administrada en sucesión inmediata), puede ser eficaz para la prevención previa a la exposición durante seis meses. Por otro lado, no está autorizado para el tratamiento de COVID-19 o para la prevención post-exposición de covid-19.
✕
Accede a tu cuenta para comentar




