CE
La Audiencia Nacional rechaza investigar el caso de las prótesis PIP
Descarta la competencia al no apreciar un delito contra la salud pública en los implantes defectuosos
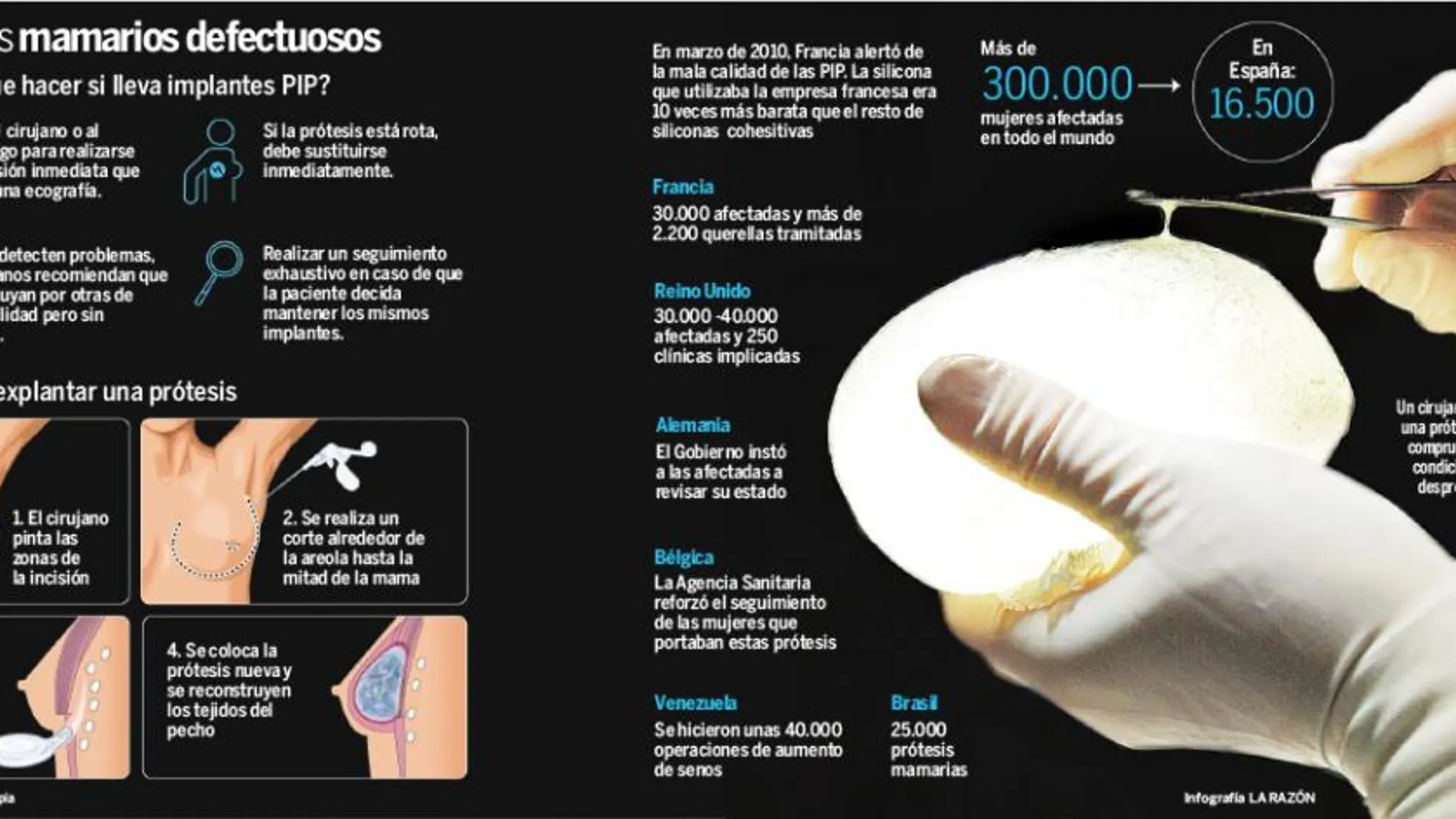
Ni los hechos pueden ser considerados un delito contra la salud pública ni han sido cometidos por un grupo organizado. Con estos argumentos, el juez de la Audiencia Nacional Javier Gómez Bermúdez ha inadmitido a trámite la querella interpuesta por 24 mujeres afectadas por las prótesis mamarias defectuosas (con un elevado riesgo de rotura) contra el fabricante de los implantes, Jean-Claude Mas, y los profesionales sanitarios que realizaron las intervenciones quirúrgicas en España por un delito de lesiones imprudentes.
El titular del Juzgado de Instrucción número 3 considera en su resolución –a la que ha tenido acceso LA RAZÓN– que este tribunal carece de competencia objetiva para hacerse cargo de la investigación, por lo que en su opinión «deberían ser los juzgados territoriales los que instruyan». Sólo si a lo largo de la misma se constatara la existencia de una organización o grupo criminal, añade, esos juzgados deberían inhibirse en favor de la Audiencia Nacional. Esta decisión no cierra la puerta a la vía penal a estas reclamaciones, sino que las deriva a los distintos juzgados de los lugares donde se llevaron a cabo los implantes.
La Fiscalía de Albacete defendió el pasado mayo, sin embargo, la competencia de la Audiencia por la pluralidad de perjudicadas «residentes en diversas poblaciones del territorio nacional» y estar ante «un supuesto fraude de sustancias farmacéuticas o medicinales cometido por una organización en la que se incluyen los proveedores en España».
La defensa de las 24 afectadas por los implantes PIP (Poly Implant Prothese), ejercida por el abogado Marcos García Montes, esgrimió en su denuncia que la competencia de la Audiencia Nacional se sustentaba en el artículo 5,1 d) de la Ley Orgánica del Poder Judicial, que incluye entre las atribuciones de este tribunal los «fraudes alimentarios y de sustancias farmacéuticas o medicinales siempre que sean cometidos por bandas o grupos organizados y produzcan efecto en lugares pertenecientes a distintas audiencias».
Para el juez, la prótesis de gel de silicona supuestamente fraudulenta (que en España se han implantado 16.500 mujeres, de las que 1.600 se han tenido que retirar, la mayoría por roturas) «no es un medicamento» en el sentido utilizado por los artículos del Código Penal que recogen el delito contra la salud pública (361 y 362,1).
Producto sanitario
El magistrado alude a la diferenciación entre medicamento y producto sanitario que establece la Ley de Garantías y Uso Racional de los Medicamentos y Productos Sanitarios de 26 de julio de 2006. Ambos difieren, subraya, «tanto por su composición como por su destino». Mientras que el primero siempre tiene una función curativa, el concepto de producto sanitario es más amplio, contempla más finalidades y la propia ley «excluye expresamente el ámbito del medicamento». La norma citada lo define como «cualquier instrumento, dispositivo, equipo, material u otro artículo» destinado a ser utilizado en seres humanos siempre «que no ejerza la acción principal que se desee obtener» en el cuerpo humano «por medios farmacológicos, inmunológicos ni metabólicos».
Para la Audiencia Nacional, por tanto, los hechos no constituyen un delito contra la salud pública en la modalidad de fabricación de medicamentos manipulados, alterados o caducados o alteración posterior a su fabricación, por lo que, «aun en la hipótesis de que se hubiera actuado a través de una banda o grupo organizado, no procedería admitir la querella por esta vía». Respecto al delito de lesiones invocado por las querellantes, Gómez Bermúdez recuerda que la Audiencia sólo es competente si se comete por españoles en el extranjero cumpliendo determinados requisitos de los que en la denuncia «no existe vestigio alguno ni en la exposición de hechos ni en su fundamentación jurídica».
Las consideraciones de la Audiencia no son compartidas por algunos cirujanos plásticos. «Mi opinión personal, sin ser un experto en Derecho, es que sí se trata de un delito contra la salud pública. ¿Qué diferencia hay entre un antibiótico en mal estado y unas prótesis como éstas, fabricadas con una silicona no apta para el uso médico?», declaró a este diario José Vilar Sancho, miembro de la International Society of Aesthetic Plastic Surgery.
«Pero los médicos no somos culpables de nada. Fue una negligencia por parte de las organizaciones sanitarias europeas –añadió– que no ejercieron su labor de vigilancia y homologaron los productos. El mismo Ministerio de Sanidad debería haber demandado al fabricante y a la Sanidad francesa. Ni médicos ni pacientes tenemos culpa de nada. Nosotros compramos unas prótesis con el sello CE, fue una adquisición legar, pagamos el IVA...»
Por su parte, Carlos Vázquez, presidente de la Sociedad Española de Senología y miembro del Comité de la Comisión Europea para el estudio de la problemática de las PIP, aseguró que «esto no deja de ser un problema con un producto mal fabricado, un frauide, un engaño para todos. No sé si es un delito hacia la salud pública». Vázquez confirma que ya está listo el registro de las 1.600 prótesis PIP ya retiradas. Éstas se han examinado y en los próximos días se van a presentar esos datos.
Régimen de control europeo
El proceso de control de calidad de las prótesis se realiza en dos fases y se rige por normativa europea. Para empezar, el fabricante debe presentar toda la documentación del producto, como el tipo de componentes, las pruebas de seguridad y los ensayos clínicos a los que se ha sometido. Con ello, un organismo evaluador, como la Agencia del Medicamento (Aemps), analiza y comprueba que toda esa información es la correcta. Después, se realiza una auditoría para examinar el lugar en el que se fabrica y comprobar que sigue los procesos de control y seguridad establecidos. De cumplir con la normativa, la Aemps otorga la autorización al fabricante y se le da el sello CE, para exportar a la UE.
✕
Accede a tu cuenta para comentar