
Ingeniería
Un colorante alimentario para imprimir órganos en 3D
Usan el sustituto químico del azafrán con hidrogeles biocompatibles para facilitar la circulación sanguínea de los tejidos más complejos
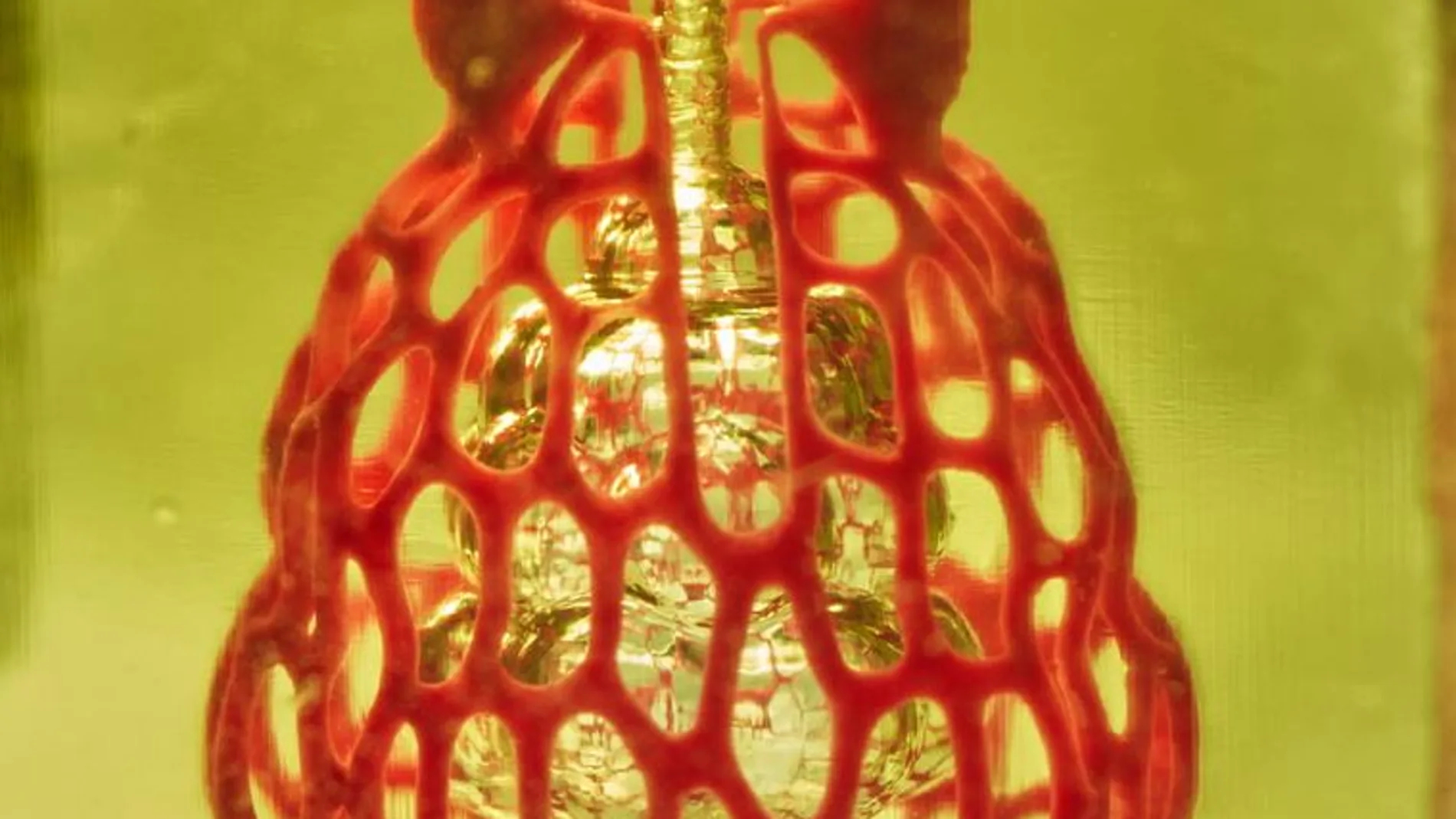
A través de un colorante alimentario se podrán imprimir órganos en 3D
A muchos seguro que no les suena la tartracina, que en las etiquetas de alimentos aparece como código E102, en la Unión Europea o Yellow 5, en EE UU. Se trata de un colorante artificial, amarillo intenso, ampliamente empleado en la industria alimentaria, que aparece, entre otros lugares, en arroces –ya que es el sustituto ideal del azafrán–, en refrescos, apertitivos, pastillas de caldo... Pues bien, la Ciencia le ha encontrado un nuevo uso como «ingrediente» en la fabricación de órganos en 3D. ¿Cómo y por qué?
Un estudio, publicado esta semana en «Science», presenta a la tartracina o E102 como el componente secreto de los biomateriales de impresión 3D con complejas redes físicamente entrelazadas, que caracterizan a los tejidos biológicos. En las capas de las vísceras sólidas se mueven fluidos y se intercambian materiales a través de redes vasculares distintas, pero biofísicas y bioquímicamente conectadas. La ingeniería de esta vasculatura en materiales biocompatibles empleados para tejidos en crecimiento constituye todavía un gran desafío a solventar para conseguir la viabilidad de los órganos impresos.
Complejo sistema
Una forma de crear estructuras artificiales capaces de imitar la compleja arquitectura vascular de los tejidos biológicos, como las que se encuentran dentro del pulmón, es a través de un tipo de impresión 3D llamada estereolitografía de proyección. La técnica utiliza luz proyectada y resinas fotorreactivas para crear objetos sólidos. Los aditivos que absorben la luz pueden usarse para detener la fotopolimerización no deseada fuera de la zona marcada, para así garantizar una resolución suficiente para la creación de arquitecturas complejas. Sin embargo, los químicos comunes empleados para este propósito son carcinógenos genotóxicos conocidos y no cumplen con los estándares para la biofabricación. La identificación de fotoabsorbentes no tóxicos útiles en este proceso podría superar una limitación importante en el diseño y generación de hidrogeles biocompatibles.
Ahora, Bagrat Grigoryan y Jordan Miller, principales responsables del estudio y sus compañeros de la Universidad de Rice en Houston (EE UU), muestran que los colorantes alimentarios naturales y sintéticos ampliamente utilizados se pueden usar como potentes absorbentes de luz en la producción de redes vasculares intrincadas y funcionales dentro de los hidrogeles. En este sentido, los investigadores de Rice junto con los de la Universidad de Washington en Seattle, Duke en Durham y Rowan en Glassboro, han evaluado el empleo de la tartrazina, o Yellow 5, como un aditivo que bloquea la luz para crear rápidamente complejos hidrogeles multivasculares. Los autores del trabajo han conseguido demostrar las capacidades funcionales de los materiales mediante la recreación de procesos biológicos, como la oxigenación de células sanguíneas en el pulmón, por ejemplo. «Uno de los mayores obstáculos para generar reemplazos de tejidos funcionales ha sido nuestra incapacidad para imprimir toda la compleja vasculatura que puede suministrar nutrientes a los tejidos densamente poblados», explica Miller, profesor asistente de bioingeniería en la Escuela de Ingeniería Brown de Rice.
«Nuestros órganos en realidad contienen redes vasculares independientes, como las vías respiratorias y los vasos sanguíneos del pulmón o los conductos biliares y del hígado. Estas redes interpenetrantes están enredadas física y bioquímicamente, y la arquitectura en sí está íntimamente relacionada con el tejido. Estamos ante la primera tecnología de bioimpresión que aborda el desafío de la multivascularización de forma directa e integral», añade Miller.
Por otro lado, con esta técnica los científicos optimizaron el tejido del hígado con bioingeniería y lo trasplantaron con éxito en un modelo de ratón de lesión hepática crónica para resaltar el potencial del método. «El hígado resulta especialmente interesante porque realiza unas 500 funciones alucinantes, probablemente sólo superadas por el cerebro. La complejidad del mismo significa que actualmente no hay una máquina o tratamiento que reemplace todas sus funciones cuando falla. Órganos humanos bioimpresos podrían algún día suministrar esa terapia», apunta Stevens.
Necesidad real
El objetivo de la bioimpresión de órganos sanos y funcionales está impulsado por la necesidad de trasplantes, que muchos países acusan (no tanto en España por su sistema eficiente). Sólo en Estados Unidos, más de 100.000 personas se encuentran en las listas de espera para trasplantes, y las que tiene la suerte de recibir ese órgano donado han de enfrentarse a toda una vida de medicamentos supresores del sistema inmunitario para prevenir el rechazo de la víscera.
El responsable de la investigación explica que en su laboratorio ya emplean el nuevo diseño y las técnicas de bioimpresión para estudiar estructuras aún más complejas, y subraya que «sólo estamos al comienzo de un viaje que explora las arquitecturas que se encuentran en el cuerpo humano. Todavía tenemos mucho que aprender». La bioimpresión ha atraído un gran interés en la última década porque, en teoría, podría abordar ambos problemas al permitir que los médicos impriman «repuestos» a partir de las propias células de un paciente. Se podría desplegar un suministro listo de órganos funcionales para tratar a millones de pacientes en todo el mundo. «Prevemos que la bioimpresión se convertirá en un componente importante de la Medicina en las próximas dos décadas», concluye Miller.
✕
Accede a tu cuenta para comentar




