
Química
¿Quieres ver un átomo? Te lo enseñamos
Aunque no lo parezca, ya tenemos microscopios tan potentes como para ver un átomo en directo. ¿Quieres ver cómo es?

Siempre que hablamos de los átomos nos queda cierto componente abstracto. Es difícil de evitar, ya que la mayoría de lo que sabemos de ellos lo obtenemos por métodos indirectos y no fácilmente visibles. Un gráfico fue la demostración del bosón de Higgs, y los libros de texto de química están llenos de dibujos, esquemas y pocas fotografías. Pero a pesar de esta abstracción, lo cierto es que sí tenemos herramientas para poder ver los átomos, y recientemente incluso hemos conseguido grabarlos en vídeo. Veamos cómo se logra lo que parece imposible.
A required part of this site couldn’t load. This may be due to a browser
extension, network issues, or browser settings. Please check your
connection, disable any ad blockers, or try using a different browser.
Bajando a la resolución atómica
Si queremos ver algo muy pequeño debemos introducirnos en el mundo de los microscopios. Existen muchos modelos diferentes, cada uno con su propio funcionamiento, y con sus propias limitaciones en el tamaño de lo que queremos ver. Por ejemplo, el microscopio que seguramente tengas en tu cabeza es el microscopio óptico. Es el más antiguo y permite poder contemplar objetos del tamaño de unos pocos micrómetros. Por ejemplo, nos permite ver células pero no distingue bien lo que hay dentro de ellas. Funciona gracias a la luz. La muestra se ilumina y los fotones atraviesan en parte lo que queremos ver, generando una imagen de sombras que llega amplificada a nuestros ojos gracias a las lentes.
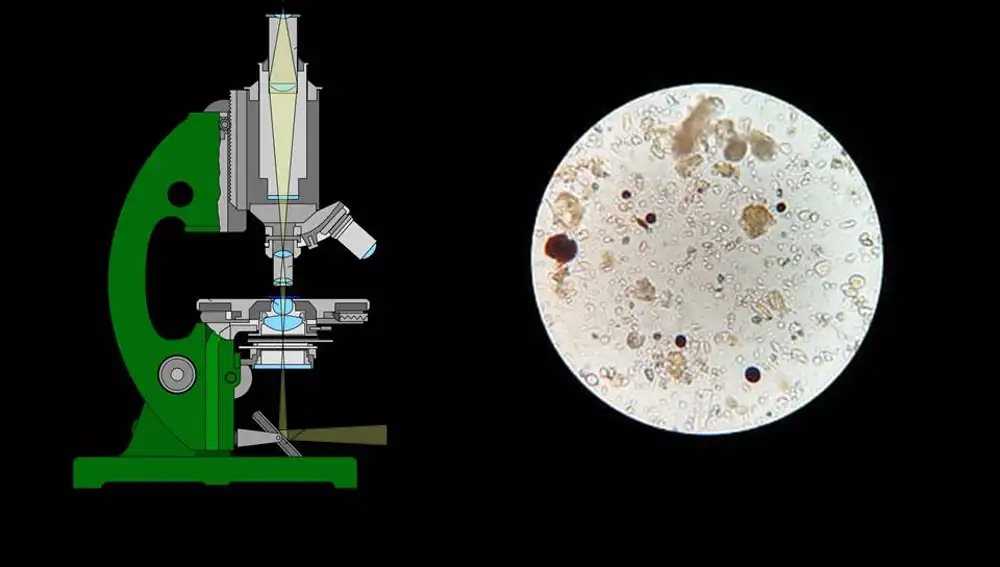
Pero estos microscopios tienen un límite de resolución, da igual lo bueno que sea o las lentes que podamos inventar. Hay que tener en cuenta que los fotones (las partículas de luz), vibran una cierta distancia mientras se desplazan, y si el objeto es más pequeño que esta vibración, los fotones distorsionan la imagen generando algo similar a una foto movida.
Si queremos una mejor resolución podemos usar un microscopio electrónico de transmisión, aunque solo está disponible en algunos centros de investigación. Se llama electrónico no por estar conectado a un ordenador (que lo está) sino porque sustituye el haz de luz por un haz de electrones. Los electrones vibran mucho menos que los fotones y nos permite ver objetos hasta cien veces más pequeños que el óptico.
Con este microscopio ya podemos ver de cerca las estructuras internas de una célula. Eso sí, lo que recibimos son electrones y nuestros ojos no están diseñados para verlos, por lo que debe estar conectado a un sensor que lee los electrones que recibe y los transforma en una imagen, que aunque sea artificial refleje la realidad.

Pero aun así, el haz de electrones es algo inestable y vibra más que el tamaño de un único átomo, por lo que no podemos usar estos microscopios para verlos. Hasta 1981 la aventura terminaba aquí. Simplemente no lográbamos lanzar nada a un átomo que nos permitiera verlo. Ni luz ni electrones.
La solución siguió otra estrategia completamente diferente. En vez de maltratar tanto a los electrones, podemos aprovecharnos de lo que sabemos de ellos. De este modo se creó el microscopio de efecto túnel.
Morse atómico
No conocemos del todo de qué están hechos los átomos, pero si tenemos alguna idea sobre su estructura más básica. Un átomo está formado por un núcleo con una cantidad determinada de protones y neutrones, y un amplio espacio reservado para los electrones, que se mueven alrededor del núcleo cual bandada de pájaros de película de Hitchcock.
Al estar moviéndose atraídos por el núcleo, los electrones tienen cierta libertad para cambiar a otro núcleo si el átomo está suficientemente cerca y tiene la carga electromagnética adecuada. Curiosamente, no sabemos del todo cómo se produce este traspaso, pero nuestras ecuaciones indican que no hay paso intermedio, que el electrón prácticamente se teletransporta de un átomo a otro. Este fenómeno recibe el nombre de efecto túnel.
Aunque no sepamos la naturaleza del efecto túnel, sí conocemos que, cuanto más cerca estén dos átomos, más posibilidades existen de que se produzca el salto. Es precisamente esa característica la que podemos usar para ver al esquivo átomo.
El microscopio de efecto tunel usa una punta de un metal conductor, tan afilada que solo tiene uno o dos átomos en su extremo. Ésta, se sitúa sobre una superficie plana pero a cierta distancia, sin llegar a tocarla. Suficientemente lejos como para que no se produzca el efecto túnel.
Al activar el microscopio la punta empieza a moverse en horizontal. Si se encuentra con un átomo que sobresalga en la superficie plana, la distancia entre la punta y el átomo será más pequeña y se transportarán electrones del átomo a la punta, recibiendo una señal. De este modo, mientras la punta se mueve podemos cartografiar la superficie, igual que cuando una persona invidente lee en braille acariciando el papel en busca de los relieves.
Podemos dejar un átomo único sobre la superficie plana y situar el microscopio encima. Metemos la señal que recibimos en el ordenador y obtendremos por fin la foto del átomo que estamos buscando.

Dada la naturaleza del método puede parecer que no tenemos mucha información sobre el átomo ni su composición. Solo parece un pequeño punto, nada parecido a lo que muestran los libros de texto. Pero el microscopio de efecto túnel tiene otras aplicaciones interesantes.
Por ejemplo, podemos usar la punta del microscopio como un pincel. Si le aplicamos un metal liquido como el mercurio, podemos depositar de manera controlada átomos individuales, logrando escribir lo que queramos. Por supuesto, esta técnica da mucho juego para generar chips de tamaño atómico. En IBM han dominado esta técnica al punto de crear un corto usando varias fotos de átomos distribuidos formando personajes y acciones.

Una limitación de este microscopio es que solo deja sacar fotos, ya que necesita un tiempo para que la punta recorra toda la superficie. Recientemente han logrado crear otro microscopio mejor, que vuelve a ser un microscopio electrónico pero con un haz de electrones tan potente que no se distorsionan a la escala atómica. Esto hace que podamos obtener información sobre los átomos microsegundo a microsegundo, generando fotogramas de un vídeo y logrando ver los átomos en movimiento.
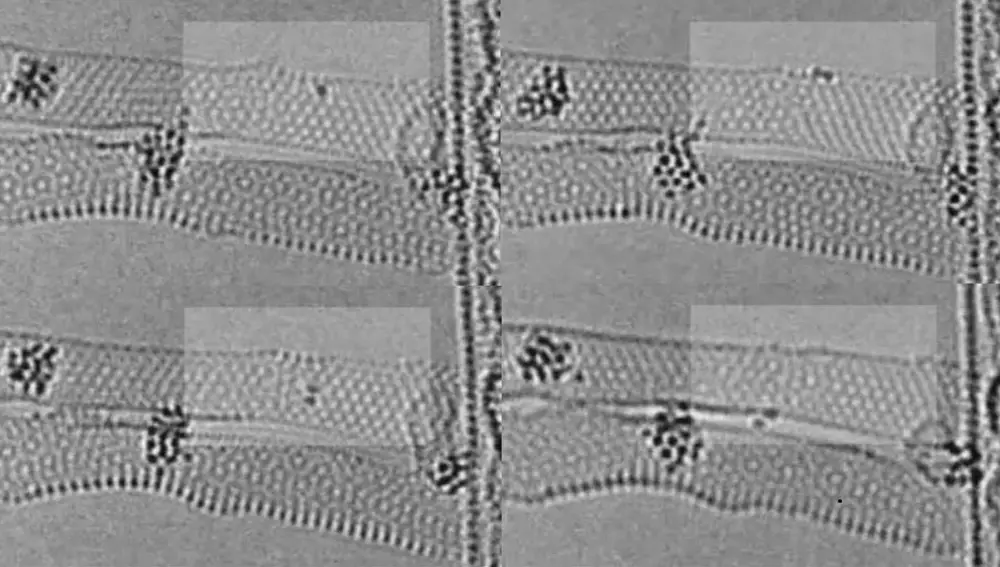
Imaginemos el gran potencial de este nuevo microscopio. Seremos capaces ver las reacciones químicas como nunca antes. No sobre el papel ni de manera teórica, sino como un vídeo que podremos disfrutar. Como demostración, en el vídeo grabado por los descubridores se puede ver un microtubo formado por átomos de Renio. De repente, dos de los átomos cercanos reaccionan entre ellos, formando una molécula de Re2 capaz de fugarse del tubo e ir a su centro. Vinimos a ver un átomo y acabamos viendo una historia de amor y fuga. La química no deja de ser sorprendente.
QUE NO TE LA CUELEN:
- Los átomos se mueven a una gran velocidad, lo que hace que estos microscopios no lleguen a captar una buena imagen de ellos.
- Los nuevos microscopios electrónicos de alta resolución necesitan anclar las moléculas que van a mirar para evitar su movimiento durante la reacción. De ahí el uso de microtubos en el vídeo.
REFERENCIAS:
- Binnig, Gerd, and Heinrich Rohrer. “Scanning Tunneling Microscopy—from Birth to Adolescence (Nobel Lecture).” Angewandte Chemie International Edition in English, vol. 26, no. 7, 1987
- Cao, Kecheng, et al. “Imaging an Unsupported Metal–Metal Bond in Dirhenium Molecules at the Atomic Scale.” Science Advances, vol. 6, no. 3, 2020
✕
Accede a tu cuenta para comentar


