
Investigación
El uso de bacterias no tóxicas en la lucha contra el cáncer
Un equipo de investigadores de EE UU ultima los detalles para poder comenzar los ensayos en pacientes en 2027
Atacar tumores con precisión intracelular es el objetivo que desde hace casi una década se ha marcado Neil Forbes, profesor de ingeniería química de la Universidad de Massachusetts Amherst, en Estados Unidos. ¿Cómo? Empleando bacterias no tóxicas en la lucha contra el cáncer.
Si en 2021 él y su equipo anunciaban en «Nature Communications» que habían logrado penetrar las membranas de las células tumorales sólidas en laboratorio, dos años después publicaban en «Frontiers in Immunology» que habían demostrado que un antígeno proteico de una vacuna infantil puede administrarse a las células de un tumor maligno para reorientar el sistema inmunológico del organismo contra el cáncer, deteniéndolo eficazmente y previniendo su recurrencia. Pues bien, ahora el equipo se prepara para los ensayos clínicos después de su último avance: utilizar aspirina en su terapia de administración dirigida de medicamentos.
El sistema de administración intracelular basado en bacterias desarrollado por este equipo de científicos, llamado BacID, utiliza una forma no tóxica de Salmonella (con expresión controlable) que libera un fármaco, en este caso un antígeno de vacuna, una vez que está dentro de una célula cancerosa de un tumor sólido. Es decir, administra medicamentos contra el cáncer en el tumor.
«El empleo de la aspirina hace que las bacterias invadan las células cancerosas. Una vez allí, se descomponen y liberan el fármaco directamente en las células», explica a este suplemento Forbes.
Las bacterias «nunca están en el ambiente fuera de las células», incide. Y es que esta tecnología emergente que regula la producción de flagelos de las bacterias y la invasión celular promete ser un tratamiento muy seguro y eficaz contra los cánceres con altas tasas de mortalidad, incluidos el cáncer de hígado (6.800 casos se diagnosticarán en 2025 en España, según las previsiones de la Sociedad Española de Oncología Médica), el de ovario (3.748 casos) y el de mama metastásico (en España cada año se detectan 35.000 casos de cáncer de cama, de los que un 30% desarrollarán metástasis: unos 10.500 pacientes).
Y eso es «porque hemos demostrado que es eficaz contra la enfermedad metastásica, que es la que mata a los pacientes en fase avanzada», aclara Forbes.
Aunque aún habrá que esperar, ya que se estima que los ensayos clínicos con pacientes oncológicos comenzarán en 2027, se trata de una noticia esperanzadora que acerca la posibilidad de «obtener un tratamiento bacteriano eficaz contra el cáncer», dice el autor principal de la investigación publicada en la revista «Molecular Therapy». De hecho, si todo va bien, podría ser realidad en «ocho años». De momento, el objetivo a corto plazo es comenzar «una pequeña prueba de fase I. Calculamos que con entre 30 y 50 personas», avanza Forbes.
«Las bacterias son el hogar natural de los tumores y, debido a que este tratamiento es tan específico, puede tratar algunos cánceres sin los efectos secundarios severos que se verían con otras terapias administradas sistemáticamente, como la quimioterapia», añade en un comunicado de la universidad el autor principal del estudio Vishnu Raman.
Para llegar hasta aquí, el equipo de científicos ha perfeccionado el desarrollo de cepas de Salmonella no tóxicas y modificadas genéticamente para atacar tumores y luego controlar la liberación de medicamentos que combaten el cáncer dentro de las células cancerosas.
«La membrana celular» de la Salmonella «fue modificada para prevenir una respuesta inmune y no produce flagelos cuando está en la sangre para prevenir aún más respuestas. Los hemos inyectado en ratones sin ninguna respuesta tóxica», asegura Forbes.
Además de evitar daños en el tejido sano, BacID tiene más potencial que la dosis administrada porque las bacterias, fáciles de fabricar, crecen exponencialmente en los tumores.
Pero, ¿por qué emplean bacterias para llevar el tratamiento? «Porque las bacterias cruzan la membrana celular y pueden administrar terapias al interior de las células. La mayoría de las otras terapias no pueden lograrlo. Cuando la mayoría de las terapias, nanopartículas o proteínas, ingresan a las células, se degradan en el lisosoma», detalla Forbes.
En este sentido, los investigadores se centraron en cómo hacer que la cepa de tercera generación fuera realmente segura y fácil de usar. «Las medidas de ingeniería genética que tomamos hicieron que esta cepa fuera al menos 100 veces más segura que cualquier otra que se haya probado en el pasado», destaca Raman.
En esta cepa, los investigadores descubrieron una forma de controlar el momento en que la bacteria, después de haber sido inyectada por vía intravenosa, invade las células cancerosas y administra el tratamiento: con la aspirina. «Administrándola tres días después de la bacteria», precisa Forbes.
Esto mejoró enormemente la capacidad de dirigirse a los tumores con concentraciones más altas de la terapia farmacológica, al mismo tiempo que hizo que el tratamiento fuera mucho más seguro.
«En la cepa de primera generación, dependíamos básicamente del propio cerebro de la bacteria para encontrar el tumor y administrar la terapia. Pero no podíamos controlar exactamente cuándo sucedía eso, por lo que existían riesgos asociados con la invasión de células sanas, así como la eliminación prematura de las bacterias antes de que colonizaran los tumores, y queríamos mitigar ambos riesgos», dice Raman.
Al principio de la investigación, los científicos descubrieron que los flagelos bacterianos (parte de la célula que ayuda al movimiento) eran los que permitían a las bacterias invadir las células cancerosas. Por ello, diseñaron un circuito genético en las bacterias que activa la producción de flagelos con una simple dosis de aspirina de venta libre.
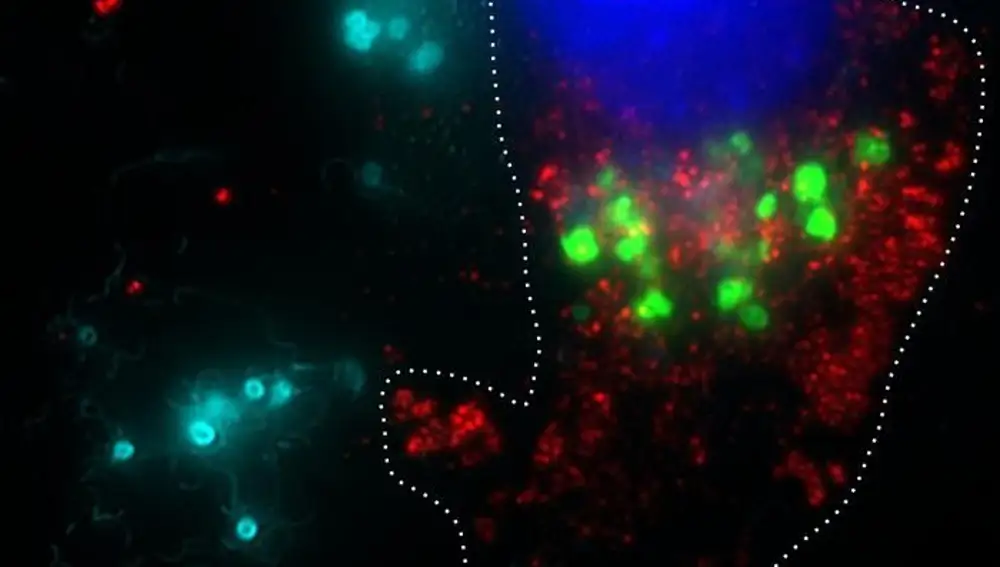
Sin el interruptor de activación que proporciona el ácido salicílico, el producto metabólico activo en la sangre después de que una persona toma una aspirina, las bacterias permanecen latentes en el tumor. En concreto, la aspirina activa el sistema BacID para expresar flagelos, invadir las células cancerosas y administrar la terapia intracelularmente.
«Un aspecto fundamental de esta tecnología es la activación controlada de los flagelos», explica Raman. «Y el otro aspecto clave es que, una vez que las bacterias entran en las células cancerosas, las diseñamos con un circuito suicida, de modo que se rompen por sí solas y liberan la terapia dentro de la célula cancerosa».
En la investigación preclínica con modelos de ratón, la bacteria se inyectó por vía intravenosa. «Se propaga por todas partes, pero luego el sistema inmunológico elimina rápidamente las bacterias atenuadas del tejido orgánico sano en dos días. Las bacterias continúan creciendo exponencialmente solo dentro de los tumores durante ese tiempo. El tercer día, administramos una dosis de aspirina de venta libre para provocar que las bacterias invadan las células cancerosas y luego administramos la terapia», dice Raman.
Resultados en ratones
Su sistema permitió en modelos de ratón con tumores aumentar la liberación de proteínas, la dispersión tisular y la colonización tumoral más de diez millones de veces.
La administración de caspasa-3 con Salmonella indujo la muerte celular en células de cáncer de páncreas, mama y hígado y redujo el crecimiento de tumores de mama. Esta cepa clínicamente lista colonizó preferentemente el tejido mamario metastásico 280 y 800 veces más que el tejido sano circundante en el pulmón y el hígado, respectivamente. Y, «en algunos ratones, eliminó todos los tumores», afirma Forbes.
Al controlar con precisión la colonización tumoral y la invasión celular, esta cepa, según los autores, supera las limitaciones críticas de la terapia bacteriana y permitirá el tratamiento de muchos cánceres difíciles de tratar y hacerlo fácil para el paciente, quien tres días después de recibir la «infusión» tendrá que tomarse una simple aspirina que se convertirá en ácido salicílico en el hígado, es decir, en la molécula activa.
El equipo ahora se centra en establecer el proceso para recibir la aprobación regulatoria para comenzar los ensayos clínicos que podrían ser el pistoletazo de salida para el boom de las bacterias contra el cáncer.
A esta investigación se suma la desarrollada por un equipo de científicos de la Universidad de Columbia que en octubre de 2024 anunció en «Nature» que habían desarrollado una bacteria que enseña al sistema inmunitario a destruir las células cancerígenas.
Esta investigación abre la puerta a una clase de vacunas, las microbianas, contra los tumores y las metástasis que podrían incluso evitar futuras recidivas. Y es que la vacuna bacteriana demostró ser particularmente más eficaz que las vacunas terapéuticas contra el cáncer basadas en péptidos que se han utilizado en ensayos clínicos anteriores, al igual que también lo ha demostrado la de la Universidad de Massachusetts Amherst.
✕
Accede a tu cuenta para comentar




