
Covid-19
AstraZeneca aportará nuevos datos de su vacuna tras reconocer que estaban “desactualizados”
Las autoridades estadounidenses han puesto en duda los resultados del ensayo clínico de la vacuna de la farmacéutica británica publicados este lunes
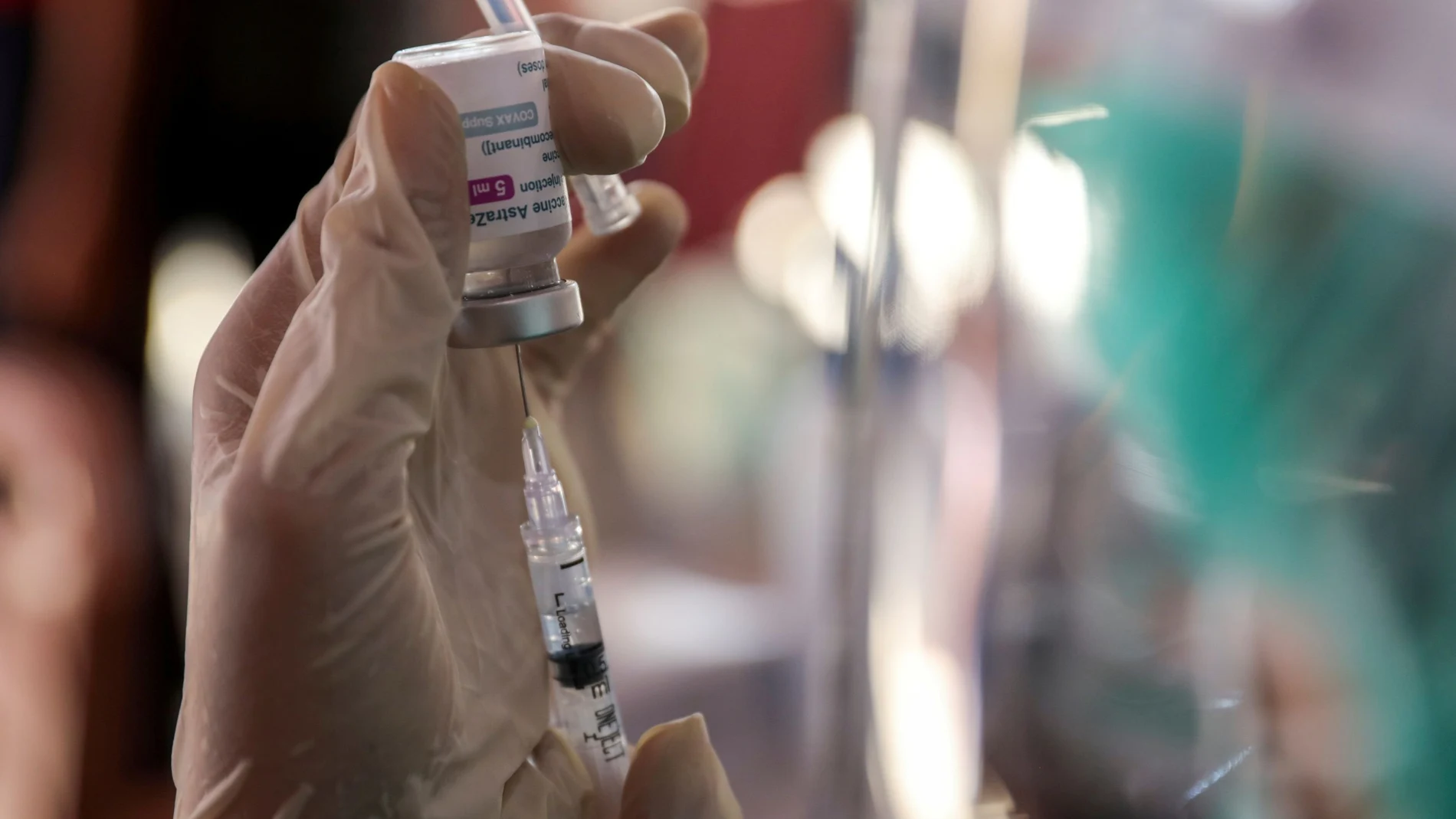
Nuevo revés a la vacuna deAstraZeneca. El Instituto Nacional de Alergias y Enfermedades Infecciosas de Estados Unidos (NIAID, por sus siglas en inglés) asegura que la farmacéutica británica podría haber facilitado información incompleta en el último ensayo realizado acerca de la eficacia y seguridad de su vacuna contra la covid-19.
El Consejo de Supervisión de Seguridad de Datos (DSMB), integrado por un panel de expertos independiente que asesora al Gobierno de Washington, ha expresado su preocupación por el hecho de que AstraZeneca pueda haber incluido “información desactualizada, que daría una visión incompleta de la eficacia de la vacuna”. Ante esta situación, la agencia estadounidense “urge” a la farmacéutica a trabajar con la organización para “revisar los datos de la eficacia y asegurar que que estas cifras más precisas y actualizadas se hagan públicas lo antes posible”.
La compañía ha respondido en un comunicado que compartirá con las autoridades sanitarias estadounidenses un análisis primario con los datos de eficacia “más actualizados” sobre su vacuna, que serán publicados “en un plazo de 48 horas”.
Este mismo lunes, AstraZeneca aseguró que su vacuna tiene una eficacia significativa del 79% en la prevención de la Covid-19 en pacientes sintomáticos y del 100% de eficacia en la prevención enfermedad y de la hospitalización, de acuerdo con un ensayo realizado en EEUU, Chile y Perú, y lo que resulta más importante, no provoca trombos ni es peligrosa para los mayores de 65 años.
Las dudas surgidas ahora pueden retrasar los planes de la compañía, que había solicitado a EE UU permiso para que su vacuna pueda ser utilizada en el país. La autorización y las pautas para el uso de la vacuna en los Estados Unidos serán determinadas por la Administración de Alimentos y Medicamentos (FDA) y los Centros para el Control y la Prevención de Enfermedades (CDCC) tras revisar la información aportada por los comités de expertos independientes.
La EMA no “descarta de forma definitiva” el vínculo de la vacuna y la coagulación
La vacuna de AstraZeneca, presentada al principio como un logro en la lucha contra la pandemia de coronavirus, se ha visto salpicada de dudas sobre su eficacia, las dosis y los posibles efectos secundarios.
La directora de la Agencia Europea del Medicamento (EMA), Emer Cooke, subrayó este martes que los informes clínicos y de laboratorio revisados por sus expertos no permiten todavía “descartar definitivamente un vínculo entre la vacuna de AstraZeneca contra la covid-19 y los casos” raros de coagulación sanguínea detectados en algunos países europeos.
La EMA sigue defendiendo que estos son muy pocos casos y que la vacuna sigue siendo “segura y eficaz” en la lucha contra la covid-19, una enfermedad cuya amenaza a la sociedad hace que el fármaco tenga beneficios que superan cualquiera de sus posibles riesgos.
Cooke subrayó también que se está analizando el posible riesgo de que estos casos puedan existir también con otras vacunas contra la covid-19 ya autorizadas (Pfizer/BioNtech, Moderna y Janssen), pero “hasta ahora no se ha identificado ninguna señal durante el monitoreo de seguridad”.
✕
Accede a tu cuenta para comentar





