Salud
Los médicos reclaman nuevos antibióticos ante las resistencias bacterianas
El coste humano es 2.000 vidas anuales en España, 900.000 en el mundo, y el gasto económico son 400 millones de euros al año, lo mismo que la gestión de un hospital grande

El peligro de las resistencias microbianas supone uno de los problemas de Salud Pública más importante de los últimos años. Su repercusión es tal, que ha sido objeto de debate en el Foro de Davos, en las Naciones Unidas y la Administración de Obama dibujó, incluso, un “plan de contingencia” para hacerles frente. Para responder a las preguntas que surgen entorno a este asunto, A TU SALUD reunió en una mesa a tres expertos de diferentes áreas para que aportaran su experiencia y sus puntos de vista.
Ricard Ferrer Roca, jefe del Servicio de Medicina Intensiva del Hospital Universitario Valle de Hebrón (Barcelona) y jefe del Grupo de Investigación Shock, Disfunción Orgánica y Resucitación (SODIR) del Instituto de Investigación del mismo centro (VHIR), explicó que “desde el punto del médico intensivista, en las UCI donde ejerzo mi labor asistencial, la multirresistencia complica la situación del paciente ingresado; más cuando son infecciones que nos obligan a usar espectros antimicrobianos más amplios y a tener un mayor riesgo cuando empleamos el tratamiento empírico –que se pone en marcha cuando no hay tiempo para recibir los resultados de las pruebas–, sobre todo en pacientes en estados muy críticos”.
Cifras que alarman
Además de los costes humanos, también hay que subrayar los económicos a los que aludió Rafael Cantón Moreno, jefe del Servicio de Microbiología del Hospital Universitario Ramón y Cajal (Madrid) e Instituto Ramón y Cajal de Investigación Sanitaria (Irycis): “He participado en un grupo de trabajo que ha analizado el impacto de las multirresistencias, sobre todo de las gramnegativas –pseudomonas seroquinos, acinebacter baumani, klebisiella neumonía, escherichia coli– que pueden provocar infecciones multirresistencia. Esos microorganismos cuestan al año lo mismo que abrir un gran hospital: 400 millones de euros anuales. Infección a infección, el sobrecoste puede suponer unos 20.000 euros”, apuntó Cantón. A lo que Ferrer añadió que “en Europa este problema se cobra 33.000 vidas al año, cerca de 900.000 en todo el mundo”.
Junto a ello, Diego López Mendoza, director de la División de Antiinfecciosas de MSD apuntó que “los costes van asociados a todas estas circunstancias porque el manejo del paciente es más complicado y el tratamiento empírico inicial tiene dificultades. Hay estudios que cifran, son estimaciones, que las estancias prolongadas derivadas de la resistencia, suponen un gasto de 1.500 millones de euros al año en Europa. Se estiman actualmente 900.000 muertes y, para 2050, hasta diez millones de fallecimientos a nivel mundial con un impacto estimado del PIB de 100 trillones de euros. Obviamente constituyen cifras muy apocalípticas y grandilocuentes que ayudan a dimensionar el problema”.
Quizás, uno de los temas que más preocupa a la comunidad médica reside en que “desde hace unas décadas no llegan nuevas familias de antibióticos, llegan novedades, pero no del todo disruptivas. De hecho, en los próximos años se va a cumplir con las previsiones que se marcó la Administración Obama de tener diez nuevas moléculas en 2020”, explicó desde la perspectiva de la industria López. Además, recalcó que “no sólo se trata del ámbito de salud humana, sino también animal, y eso engloba lo que se denomina “One-Health”, un concepto que se debe abordar desde el ámbito público-privado”. Mientras tanto, lo que queda es ponerse manos a la obra con el uso racional del botiquín existente.
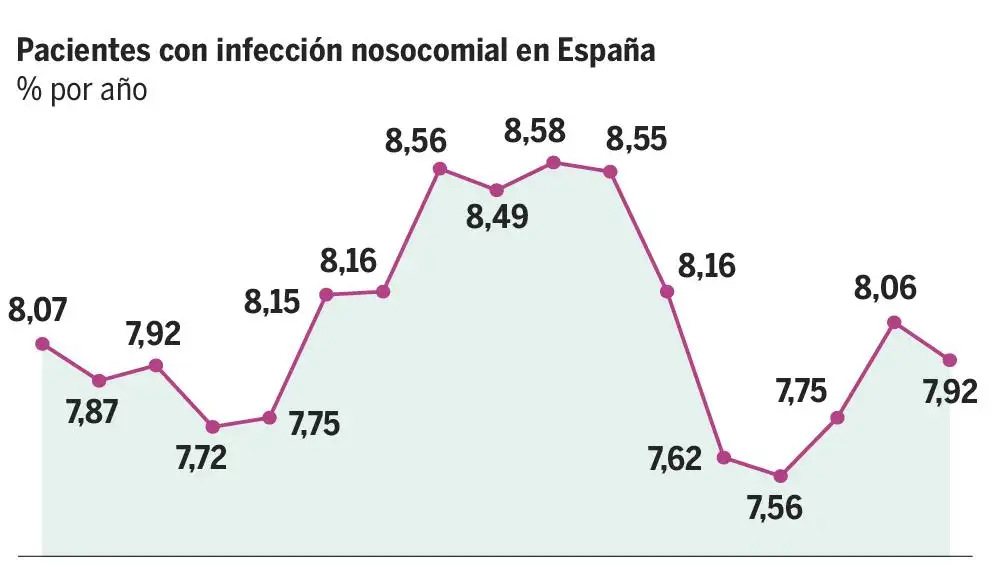
Cantón puso el foco de atención en que todo esto se observa muy bien “en el nicho ecológico hospitalario, donde se producen. Los programa de optimización de uso de antibióticos (PROA) sirven para mejorar su empleo reduciendo su impacto ecológico. También se han puesto en marcha en el ámbito extrahospitalario y en salud animal”. Por este motivo, López subrayó que el objetivo del uso racional debe apoyarse en la “individualización de los tratamientos para cada paciente, ‘‘no vale el café para todos’’. Esto tiene sentido a nivel comunitario y a nivel hospitalario. En los pacientes críticos es complicado y en el séptico resulta crucial, es donde hay que ser más preciso. Por ello, cobra sentido el trabajo multidisciplinar y el conocimiento de la ecología de cada servicio para tener más cartas para acertar. Hay que optimizar el uso de todos las opciones disponibles, dar lo mejor para su situación. Y esto genera controversias en cada caso”.
Tal como lo explica Ferrer, también presidente de la Sociedad Española de Medicina Medicina Intensiva (Semicyuc), “hay dos factores a tener en cuenta: la situación del paciente y el riesgo de multiresistencia. Si el paciente está muy grave no me puedo equivocar; si la situación no resulta tan comprometida, tengo margen de retrasar un poco el tratamiento para tener más información clínica. Al final, combinamos moléculas de muy amplio espectro para pacientes con infecciones graves con factores de riesgo de multirresistencia: un tratamiento amplio con un uso del máximo nivel armamentario. En esta situación, la comunicación con el servicio de Microbiología será fluida para que ellos analicen las muestras que solicitamos de la forma más ágil. El lema es el antibiótico más preciso y ajustado a la bacteria”.
El portavoz de MSD destacó que “el uso de los antibiótico es universal, un médico tiene capacidad de prescribir este medicamento desde que se licencia. Si bien es cierto, en los pacientes complejos hay más especialización. Hay margen de mejora, gracias a un incremento de la educación sanitaria y a la introducción y mejor manejo de las nuevas moléculas”.
Eliminar peligros
Ferrer puntualizó que una cosa a considerar son los factores de riesgo, “uno de ellos es la estancia misma en el hospital y su prolongación temporal. Así, en una UCI hay más peligro que en planta y a su vez que uno ambulatorio. Sin olvidar que hoy la extra hospitalaria entraña riesgos, como en las residencias, pacientes en diálisis... todo esto añade cierto peligro de multirresistencia”. Las barreras entre hospital y el exterior se han difuminado, como explica Cantón, porque el paciente ingresado puede ser dado de alta “colonizado por la bacteria multirresistente y puede contribuir a su diseminación, aumentado el riego de infecciones de dificil tratamiento. Por ello es importante su control. Las infecciones hoy han obligado a variar el uso que hacíamos de los tratamientos. Las infecciones hoy han variado el uso que hacíamos de los tratamientos”.
Asimismo, el jefe de Microbiología del Ramón y Cajal apuntó que “hay diferencias entre países del norte –menos resistencias– y sur a nivel global en cuanto a resistencias, por el tipo de bacteria y el antibiótico que más se usa en un país u otro. Por ejemplo, en el sudeste asiático hay más que en el área del Mediterráneo”. Y junto a ello, recalcó que uno de los objetivos debe ser “el control de la infección, la posibilidad de que se transmita o no la bacteria también resulta importante para eliminar nuevos focos”. Para López “el paciente séptico es el paradigma del enfermo infectado grave y se necesita el enfoque multidisciplinar: diagnósticos rápidos, se usan antibióticos de amplio espectro, no se escatima en esfuerzos...”. En esta línea, Ferrer añadió que “estas infecciones hay que verlas como un proceso asistencial del hospital donde participan diferentes especialistas y se deben valorar diferentes indicadores. A veces en los recortes de gastos, se eliminan recursos de los laboratorios que empeoran el funcionamiento de este proceso”.
Todo ello será, y es en algunos casos, optimizado por las nuevas tecnologías. “El ‘‘machine learning’’ debería ser de uso obligatorio, pero no hay figuras de ‘‘data science’’ aún en los hospitales”, recalca Ferrer. A lo que Cantón añade que “estas herramientas facilitarían la recogida de datos y su interpretación y nos ayudarían a manejar datos más ajustados a la realidad”. Pero todo ello retorna a un punto en el que se une a la falta de inversión: tanto en moléculas antiinfecciosas como en el área de digitalización sanitaria. “Se necesita de mucha innovación en este terreno y hacer más trabajo de difusión de lo que supone apostar por ello y las repercusiones que tiene”, concluye López.
✕
Accede a tu cuenta para comentar