Oncología
«Es necesario ampliar los centros que utilizan CAR-T»
En España sólo hay diez hospitales cualificados para su administración

«Considero necesario ampliar el número de hospitales que ofrecen la terapia CAR-T en España». Así lo entiendeJavier de la Rubia, jefe del Servicio de Hematología del Hospital La Fe, de Valencia, para quien, hasta ahora, se había emprendido una estrategia conservadora, con unos pocos centros en todo el territorio nacional para que la desarrollaran, «lo que para empezar está bien, pero, a medio plazo, habría que sumar más centros a los 10 que la aplican en nuestro país, ya que hay comunidades que no cuentan con ninguno y muchos pacientes tienen que desplazarse para poder recibirla», continúa el experto.
Los extraordinarios resultados obtenidos hasta ahora con este tratamiento no sólo llevan a pensar en ampliar el número de centros donde se aplica, sino también las patologías a tratar. Y es que, aunque por el momento esta nueva generación de inmunoterapias avanzadas se emplea contra cánceres hematológicos, en los próximos meses habrá noticias sobre su aplicación en otros como el de las células del manto; y más adelante, se verá cómo emplear la terapia génica CAR-T en tumores sólidos. «Está también muy avanzado su desarrollo en mieloma múltiple, y es muy posible que la Agencia Europea del Medicamento (EMA) apruebe su uso en 2022, así como en otros síndromes linfoproliferativos, como la leucemia aguda mieloplástica», asegura De la Rubia.
Hasta la fecha, la Comisión Europea ha autorizado la comercialización de los dos primeros medicamentos con células CAR-T de fabricación industrial: axicabtagén ciloleucel, para el tratamiento de adultos con linfoma B difuso de células grandes refractario o en recaída y linfoma B primario mediastínico de células grandes y, tisagenlecleucel, para pacientes pediátricos y jóvenes con leucemia linfoblástica aguda B y linfoma B difuso de células grandes. Además, recientemente, la Comisión ha concedido la autorización de comercialización condicional a brexucabtagene autoleucel para pacientes adultos con linfoma de células del manto en recaída o refractario después de dos o más líneas de terapia sistémica.
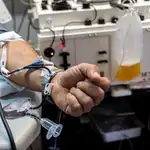
Los CAR-T son medicamentos de terapia celular basados en la modificación genética de los linfocitos T del paciente que se extraen mediante un proceso de aféresis y, posteriormente, se modifican de manera casi artesanal para que, una vez infundidas de nuevo al paciente, identifiquen y ataquen a las células cancerosas. Es un proceso complejo, ya que cada tratamiento se elabora de manera individualizada para cada paciente.
«Nuestra experiencia con ellos es muy buena y todos los enfermos que hemos tratado con CAR-T, tras un año de seguimiento, que es el tiempo que hemos tenido para ello, están libres de enfermedad y asintomáticos (a excepción de uno que falleció) y sin toxicidad grave a largo plazo, lo que, teniendo en cuenta que eran pacientes sin otra alternativa terapéutica, es revolucionario», concluye De la Rubia.
¿Cuántos casos se han tratado?
El Ministerio de Sanidad trabaja desde 2018 en un plan específico de abordaje de la terapia celular enmarcado en el Plan Estratégico de Medicina de Precisión, para definir e impulsar la implantación de estos fármacos en el Sistema Nacional de Salud. Desde marzo de 2019 y hasta octubre de 2020, ha recibido 386 solicitudes de tratamiento con terapias CAR-T, y se han tratado a 182 pacientes (el 89% de las recibidas).
✕
Accede a tu cuenta para comentar