
Covid-19
La EMA avala la vacuna de Pfizer contra las variantes Ómicron en niños de 5 a 11 años
También ha autorizado un suero de Sanofi Pasteur como refuerzo en adultos
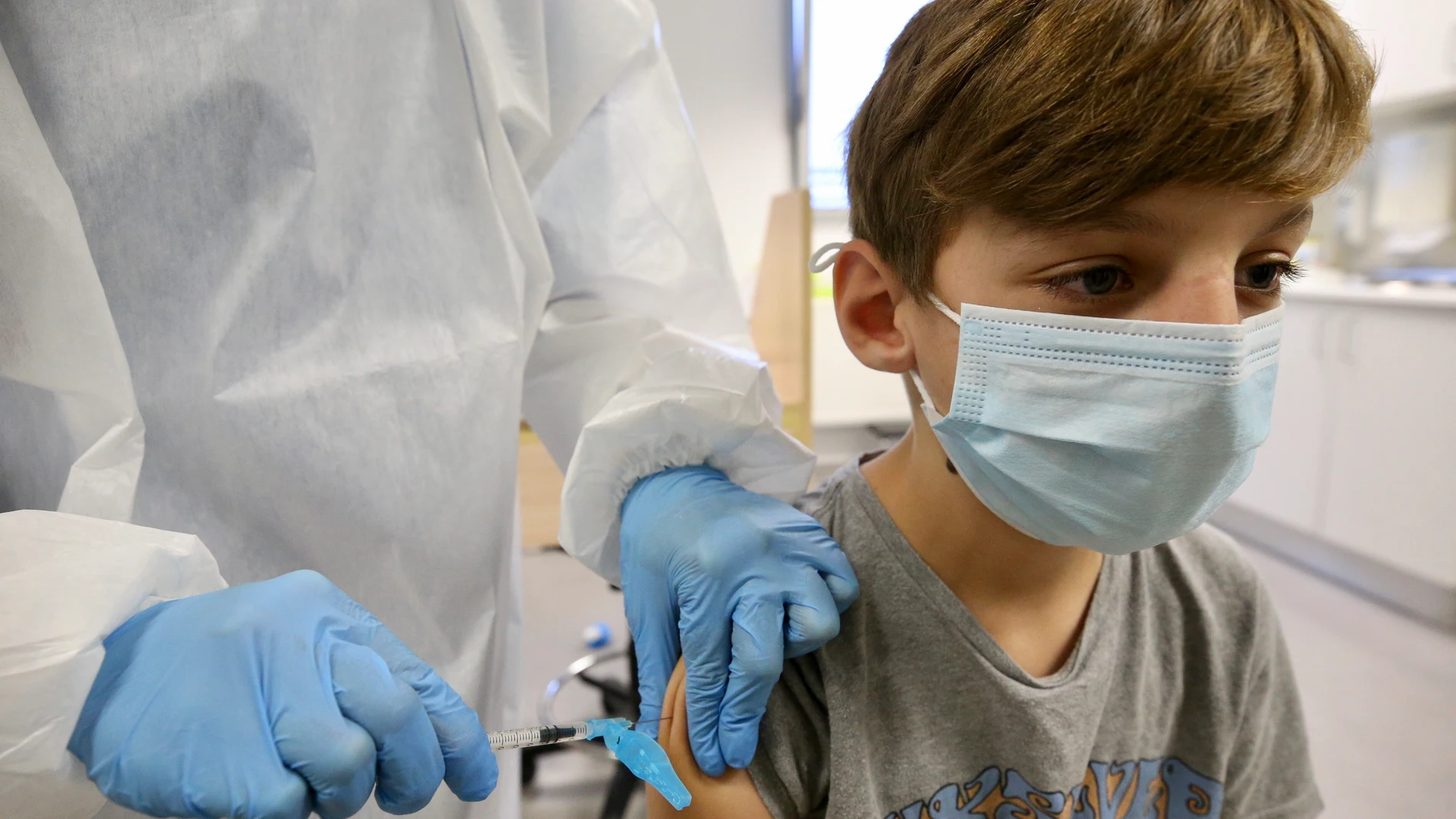
El Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea de Medicamentos (EMA, por sus siglas en inglés) ha dado su visto bueno a la vacuna de Pfizer contra las variantes BA.4 y BA.5 de Ómicron para niños de entre 5 y 11 años. La Comisión Europea revisará ahora la recomendación del CHMP y se espera que tome una decisión final para su aprobación definitiva “en breve”, informa Ep.
La vacuna bivalente adaptada a BA.4 y BA.5 está actualmente autorizada en la Unión Europea (UE) como dosis de refuerzo para personas de 12 años o más.
La recomendación del CHMP de incluir a los niños de 5 a 11 años de edad se basa en los datos de seguridad e inmunogenicidad de la vacuna bivalente contra la subvariante BA.1 en personas de 12 años o más, datos de la formulación pediátrica de la vacuna original, datos de fabricación de la formulación pediátrica en la vacuna contra BA.4 y BA.5 y datos preclínicos de la vacuna bivalente adaptada a BA.4 y BA.5.
Los datos clínicos de un ensayo de fase 2/3 de la vacuna bivalente adaptada a BA.4 y BA.5 en mayores de 18 años demostraron una fuerte respuesta inmunitaria contra estas dos subvariantes hasta 30 días después de la inmunización, con un perfil de seguridad y tolerabilidad similar al de la vacuna original de Pfizer.
Además de este ensayo y de los datos ya presentados, está en marcha un estudio pediátrico de fase 1/2/3 que evalúa diferentes regímenes de dosificación y niveles de dosis de la vacuna bivalente adaptada a BA.4 y BA.5 en todos los grupos de edad. Los datos de estos dos ensayos “se compartirán con las autoridades reguladoras de todo el mundo tan pronto como estén disponibles”, según han avanzado las compañías.
Nuevo suero de refuerzo
Por otra parte, la EMA ha autorizado también la vacuna VidPrevtyn Beta, desarrollada por el laboratorio francés Sanofi Pasteur, como dosis de refuerzo contra la Covid-19 en adultos ya vacunados con un suero de ARNm.
La Agencia Europea inició el pasado marzo la evaluación de la solicitud de licencia de Sanofi Pasteur, pero ahora sus expertos han concluido que disponen de datos suficientemente sólidos sobre la calidad, la seguridad y la inmunogenicidad de la vacuna para recomendar su autorización de comercialización en la Unión Europea (UE), señala Efe.
“Se espera que una dosis de refuerzo de VidPrevtyn Beta sea al menos tan eficaz como Comirnaty (nombre comercial de la vacuna de Pfizer) para restablecer la protección frente a la Covid-19″, aseguró la EMA.
Esta vacuna se basa en una versión cultivada en laboratorio de la proteína espiga que se encuentra en la superficie de la variante Beta del virus SARS-CoV-2 y contiene un “adyuvante”, una sustancia que ayuda a fortalecer las respuestas inmunitarias a la vacuna.
Los efectos secundarios más comunes observados con esta vacuna fueron dolor en el lugar de la inyección, dolor de cabeza, muscular o articular, malestar general y escalofríos pero, por lo general, estos eran leves y desaparecen en un par de días después de la vacunación.
La EMA enviará ahora sus recomendaciones a la Comisión Europea, que es quien tiene la última palabra sobre la autorización de las vacunas en la Unión Europea.
✕
Accede a tu cuenta para comentar





