
Ciencia
Cómo crear un medicamento nunca antes visto
Crean una colección de pequeñas moléculas tridimensionales que permitirá generar nuevos medicamentos

Muchos medicamentos provienen de la naturaleza. Un animal, una corteza, o un hongo pueden esconder en su interior alguna molécula química capaz de afectar a nuestro organismo. En ocasiones algún compuesto que actúa como veneno en altas concentraciones puede tener un efecto antitumoral o antibiótico en la concentración justa. Por ejemplo, algunos hongos secretan sustancias antibióticas que no hemos dudado en aislar para nuestro uso personal, como la penicilina.
Pero, ¿qué pasa si queremos un medicamento completamente nuevo? Algo que no existe en la naturaleza y no podemos inspirarnos en ninguna molécula conocida. En este caso, debemos adentrarnos en la química farmacéutica y sus estrategias para hacer un medicamento desde cero.
Apuntando a la diana
Para empezar, necesitamos una diana. Así se le llama a la proteína a la que queremos afectar a través de la unión de nuestra molécula. Dependiendo de la diana, estaremos buscando un tipo de medicamento u otro. Por ejemplo, si nuestra molécula consigue unirse a alguna proteína implicada en el crecimiento y proliferación de una bacteria patógena e inhibir su funcionamiento, tendremos un posible antibiótico.
Este posible medicamento candidato, luego, tendrá que pasar por toda una serie de ensayos clínicos y de seguridad. Primero se probará a través de cultivos celulares, luego en animales de experimentación y finalmente de humanos. Un arduo proceso en la que la mayoría de candidatos son descartados. Se calcula que aproximadamente por cada diez mil candidatos, solo uno será suficientemente efectivo y con pocos efectos secundarios como para que merezca la pena. Por ese motivo, cuantos más candidatos nuevos podamos encontrar, es más probable que obtengamos algún nuevo medicamento escondido a simple vista.
Una proteína consiste en una larga cadena o varias cadenas de aminoácidos, retorcidas en el espacio formando una estructura tridimensional. No todas las partes de esta estructura serán igual de importantes: en algunas unir una pequeña molécula no tendrá ningún efecto, pero en otras provocaremos una interferencia en el funcionamiento normal de la proteína. A estos puntos se les llama regiones activas, y normalmente son huecos que tienen un tamaño y carga determinado. Por ejemplo, si una proteína funciona a través de la unión con el oxígeno, tendrá una región activa con la forma perfecta para unir esa molécula, una plantilla en negativo que le encaja como un guante.
Si realmente queremos afectar al funcionamiento normal de la proteína diana, debemos buscar moléculas que se encajen en esos mismos huecos, bloqueando, compitiendo o desplazando al compuesto que debe unirse de manera habitual.
Si tenemos bien estudiada la proteína, entonces podemos saber la forma exacta de ese hueco e incluso podemos modelizarlo en el ordenador. De este modo podemos simular cómo sería la unión de diferentes moléculas candidatas sin necesidad de hacer ningún experimento. Aunque finalmente estas candidatas son probadas en la vida real y a veces traen sorpresas, el hecho de poder experimentar a bajo coste lo hace la técnica favorita para muchos laboratorios y empresas farmacéuticas.
Pero pongámonos en el peor caso: no conocemos bien la forma de la proteína diana y sus regiones activas. Los motivos pueden ser varios. Puede que la proteína tenga alguna estructura móvil que cambie con facilidad. O puede que la ciencia básica no haya tenido los recursos o el tiempo para descubrir su forma. Para estos casos, se usa una estrategia llamada “descubrimiento dirigido a través de fragmentos”. La idea, a priori, es sencilla: Si no conocemos qué moléculas funcionan contra la diana, probemos todas.
Prueba y error
Aunque puede parecer una locura ya que existen una infinidad de combinaciones de moléculas en el mundo, podemos darle una oportunidad. Lo cierto es que, si nos fijamos, muchas moléculas tienen una forma parecida entre sí. Si buscamos encajar en el hueco de la región activa, podemos ir probando con fragmentos pequeños, ver los que se ajustan mejor y provocan un efecto. Luego jugamos a ir modificándolos y haciéndolos crecer poco a poco.
De este modo, el fragmento pequeño inicial funciona como un árbol de navidad, al que vamos añadiendo modificaciones. Podemos cambiar un átomo de hidrogeno por uno de litio, que es un poco más grande. O añadir un pequeño anillo aromático de átomos de carbono que le da una estabilidad mayor a cambio de un mayor tamaño de la molécula en su extremo izquierdo. Con cada cambio se comprueba si ha tenido algún efecto en la diana, buscando siempre maximizarlo.
Esta estrategia es larga y requiere de muchas repeticiones de prueba y error, pero sigue siendo más barata y rápida que probar moléculas al azar. Poco a poco se obtiene una molécula candidata que consigue afectar a la diana con un buen éxito, y de hecho, los pasos intermedios también se aprovechan como candidatos posibles.
Este sistema lleva usándose los últimos diez años y con bastante buen éxito. Varios antitumorales en el mercado se han creado de esta manera, situando como diana proteínas que están especialmente presentes en las células tumorales.
Para hacer esta técnica, los laboratorios usan una mezcla de moléculas orgánicas ya establecida, que incluye entre 100 y 1000 moléculas muy diferentes entre sí. Todas ellas tienen un tamaño pequeño pero una gran variedad en su composición y forma, asegurando maximizar las posibilidades de encontrar alguna molécula candidata… pero hay un problema: la mayoría de estas moléculas son planas.
Esta preferencia por lo plano proviene de la propia química orgánica. Las moléculas orgánicas están formadas principalmente por cadenas de enlaces entre carbono e hidrógeno, y aunque algunas tengan capacidad para rotar y girar como una serpiente, suelen crecer de manera bidimensional. No es fácil ver moléculas orgánicas con la forma de una pirámide doble de dos pisos.
Y esta falta de tridimensionalidad hace que nos falte un espacio químico por descubrir. Las regiones activas de la diana que queremos atacar realmente tienen tres dimensiones, y puede que existan moléculas tridimensionales que permitan actuar como andamios de medicamentos nunca vistos hasta ahora.
Un equipo de científicos estadounidenses y franceses ha trabajado en equipo para abordar este problema. Ya que la química orgánica pura no favorece este tipo de estructuras, han sintetizado una colección de moléculas metalorgánicas, que se diferencian por tener algún átomo de un metal, como cobalto o níquel. Algunos de estos átomos permiten más enlaces que el carbono y podemos construir moléculas tridimensionales con facilidad, algunos con forma de sándwich, otros con forma de pirámide. Y así hasta setenta y una moléculas, todas muy diferentes entre sí.
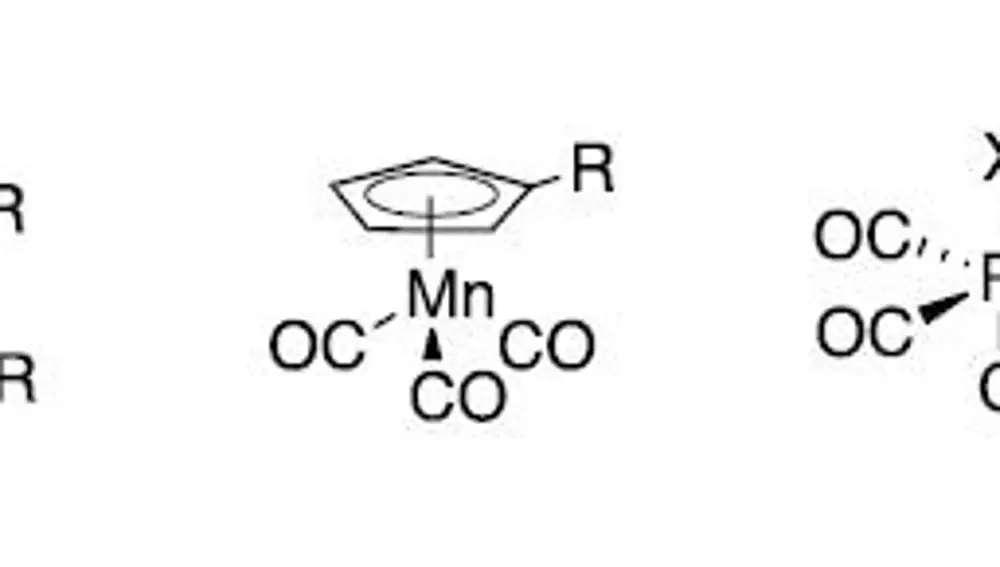
Para demostrar su potencial, probaron su colección buscando medicamentos candidatos contra tres dianas concretas: una proteína que confiere resistencias a antibióticos en bacterias, un complejo de proteínas que replica el ARN viral en la gripe A y una proteína que aparece aumentada en algunos tumores y favorece su crecimiento. En los tres casos se encontraron moléculas candidatas a nuevos tratamientos, probando al mismo tiempo su eficacia para crear medicamentos antibacterianos, antivirales y antitumorales respectivamente.
Con algo de suerte y paciencia, algunos de estos nuevos fragmentos actuarán como andamio para algún medicamento totalmente nuevo y nunca visto. Si la naturaleza no nos aporta nuevas ideas, tendremos que usar nuestro ingenio y crear formas nuevas.
QUE NO TE LA CUELEN:
- Este artículo está centrado en el primer paso para obtener candidatos a nuevos medicamentos. Luego todos estos candidatos deben pasar exhaustivas pruebas de eficacia y seguridad para poder salir a la luz.
- Aunque algunos medicamentos tengan un origen natural, en los fármacos se controla la dosis y se limpian las posibles impurezas para mejorar su eficacia. Obtener el mismo medicamento de su fuente original puede ser ineficaz en el mejor de los casos o incluso peligroso.
REFERENCIAS:
- Morrison, Christine N., et al. “Expanding Medicinal Chemistry into 3D Space: Metallofragments as 3D Scaffolds for Fragment-Based Drug Discovery.” Chemical Science, (2020)
- Scott, Duncan E., et al. “Fragment-Based Approaches in Drug Discovery and Chemical Biology.” Biochemistry, vol. 51, no. 25, pp. 4990–5003 (2012)
✕
Accede a tu cuenta para comentar


