
Neurociencias
Desarrollan un minicerebro para estudiar el trastorno del espectro autista
Un equipo internacional busca identificar las células vulnerables y las redes reguladoras de genes que están involucradas en el TEA.
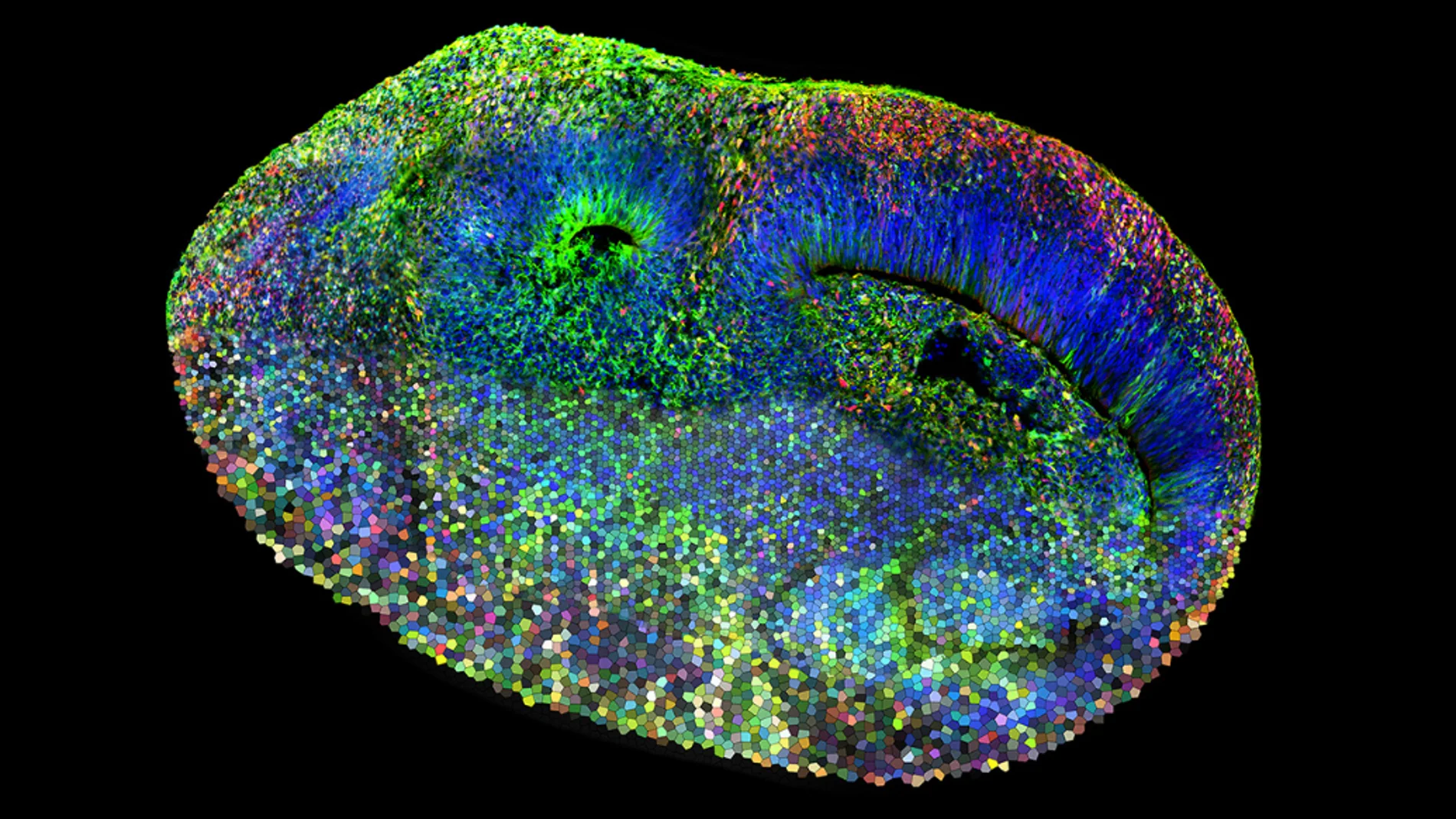
En comparación con otras especies animales, el cerebro humano, para desarrollarse, depende de procesos exclusivos. La ventaja es que nos permite construir una corteza conectada y en intrincadas capas. La desventaja es que estos mismos procesos únicos también hacen que los trastornos del neurodesarrollo sean más probables en los humanos. Por ejemplo, muchos genes que confieren un alto riesgo de desarrollar un trastorno del espectro autista (TEA) son, al mismo tiempo, cruciales para el desarrollo de la corteza. ¿Puede el desarrollo de minicerebros ayudarnos a comprender estos procesos?
Aunque los estudios clínicos han demostrado una relación de causalidad entre múltiples mutaciones genéticas y el autismo, los investigadores aún no comprenden cómo estas mutaciones conducen a defectos en el desarrollo del cerebro y, debido a la singularidad del desarrollo del cerebro humano, los modelos animales son de uso limitado. "Solo un modelo humano del cerebro puede recapitular la complejidad y las particularidades del cerebro humano", afirma el director científico del IMBA, Jürgen Knoblich, líder del equipo internacional que ha desarrollado un organoide, similar a un cerebro humano, para estudiar los mecanismos detrás del TEA.
La primera pregunta que se hizo el equipo liderado por Knoblich, formado por del grupo Knoblich del Instituto de Biotecnología Molecular (IMBA) de la Academia de Ciencias de Austria y el grupo Treutlein de la ETH Zurich es si nuestro cerebro tiene un talón de Aquiles que, en última instancia, conduce al autismo. Para responder a ello desarrollaron un sistema que combina tecnología de organoides cerebrales y genética y así probar, de manera integral, el efecto de múltiples mutaciones en paralelo y a nivel unicelular dentro de los organoides que simulan el cerebro humano. Esta tecnología, desarrollada por investigadores, permite identificar tipos de células vulnerables y redes reguladoras de genes que subyacen a los trastornos del espectro autista.
Los organoides cerebrales se desarrollaron a partir de muestras de células madre de dos pacientes. Ambos pacientes tenían mutaciones en el mismo gen que causaba el autismo. Este desarrollo es especialmente impactante porque los genes de interés pueden examinarse simultáneamente dentro de un único organoide en mosaico, lo que marca el comienzo de una era de detección genética intrincada, eficiente y conveniente en tejido humano.
En el sistema, descrito en un artículo publicado en Nature, cada célula del organoide (del minicerebro) porta como máximo una mutación en un gen específico del TEA. De este modo, el equipo de Knoblich pudo rastrear el efecto de cada mutación a nivel unicelular y mapear la trayectoria de desarrollo de cada célula. “Con esta metodología de alto rendimiento – explican los autores en un comunicado -, podemos inactivar sistemáticamente una lista de genes que causan enfermedades. A medida que crecen los organoides que portan estas mutaciones, analizamos el efecto de cada mutación en el desarrollo de cada tipo de célula. Podemos ver las consecuencias de cada mutación en un solo experimento, acortando así drásticamente el tiempo de análisis en comparación con los métodos tradicionales, utilizando un enfoque que durante décadas solo era posible en organismos como la mosca de la fruta”.
Mutar varios genes en paralelo y rastrear sus efectos genera una enorme cantidad de datos. Para analizar este complejo conjunto de datos, la coautora Barbara Treutlein y su equipo de ETH Zurich utilizaron enfoques de bioinformática cuantitativa y aprendizaje automático.
“Utilizando estos datos de expresión unicelular de alto rendimiento – añade explica Treutlein-, podemos cuantificar si un tipo de célula determinado es más o menos abundante debido a una mutación determinada, y también podemos identificar conjuntos de genes que se ven afectados común o claramente por cada mutación. Al comparar todas las mutaciones genéticas, podemos reconstruir el panorama fenotípico de estas perturbaciones genéticas relacionadas con enfermedades”.
Utilizando este sistema, los científicos han demostrado que las mutaciones de 36 genes, que se sabe que ponen a los portadores en alto riesgo de autismo, conducen a cambios específicos en el tipo de células en el cerebro humano en desarrollo. "Demostramos que algunos tipos de células son más susceptibles que otros durante el desarrollo del cerebro e identificamos las redes que son más vulnerables a las mutaciones del autismo", concluye el coautor Chong Li.
✕
Accede a tu cuenta para comentar


