
Coronavirus
Comienza la fase III del ensayo de la vacuna española contra la covid
Los hospitales que testan la desarrollada por Hipra buscan voluntarios para la última parte del estudio
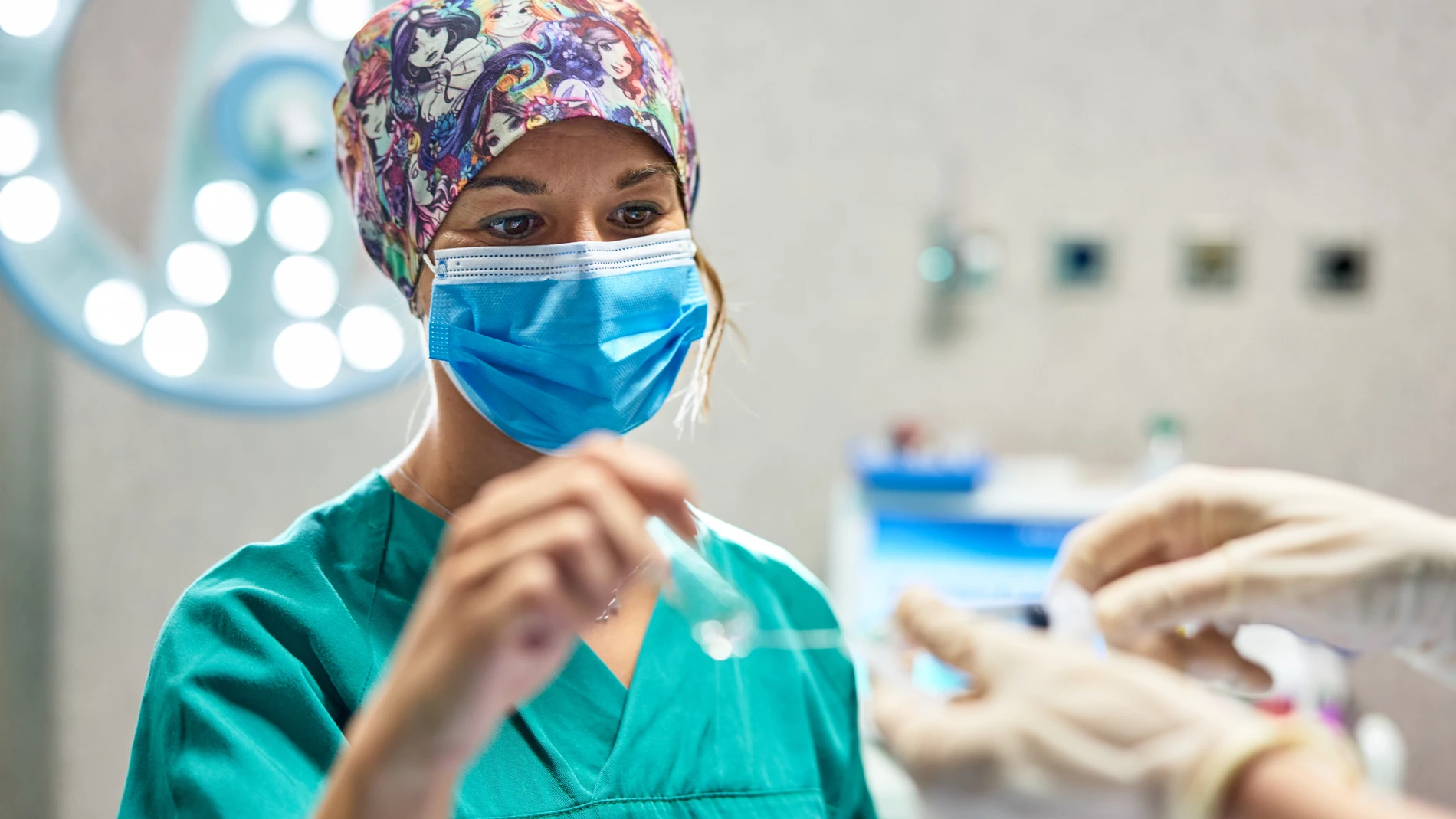
Si quiere formar parte de la historia y, al mismo tiempo, contribuir en un avance científico histórico, como lo es ser parte del estudio de la vacuna española contra el SARS-CoV-2, está a tiempo. Y es que los hospitales españoles donde se testará la que está desarrollando la farmacéutica española Hipra, y que ha alcanzado ya la fase III (la última antes de su comercialización), están buscando voluntarios con los que terminar de testar su ensayo.
Los hospitales públicos Gregorio Marañón, La Paz, Príncipe de Asturias, de Madrid, buscan voluntarios para participar en el mismo. También HM Hospitales va a integrarse en este ensayo, destinando decenas de equipos los hospitales universitarios HM Sanchinarro, HM Montepríncipe y HM Puerta del Sur (Comunidad de Madrid) y el Hospital HM Nou Delfos (Barcelona).
El estudio tiene como principal objetivo evaluar la seguridad y respuesta inmunológica de una dosis de refuerzo de la vacuna que está desarrollando la farmacéutica biotecnológica para prevenir la infección por SARS-CoV-2.
Requisitos
El requisito fundamental que deben cumplir los voluntarios que deseen participar en el ensayo reside en la necesidad de haber recibido una o dos dosis de las vacunas de Pfizer, Moderna, AstraZeneca, Janssen o combinadas, hace al menos tres meses. Del mismo modo, pueden participar en el ensayo aquellos voluntarios que han pasado la covid hace más de un mes sin haber necesitado ingreso hospitalario.
En este sentido, se han habilitado canales específicos de reclutamiento para coordinar a aquellos voluntarios comprometidos con el avance de la investigación científica en España. Los voluntarios que cumplan estos requisitos y hayan sido seleccionados serán contactados para informarles en detalle e iniciarán el ensayo, previsto para finales de enero, una vez se reciba la autorización del Comité de Ética del Hospital Clínic de Barcelona y de la Agencia Española del Medicamento y Productos Sanitarios (Aemps).
HM Hospitales vehiculizará su participación mediante la Unidad de Investigación de Vacunas, que dirige la Dra. Silvina Natalini, y que reclutará voluntarios para la participación en este ensayo clínico. “Cuando hablamos de un proyecto de vacuna frente a la Covid-19 el desafío es mayor por la relevancia que puede alcanzar para la sociedad. Además, como ha informado la farmacéutica biotecnológica, los resultados de la vacuna en las fases I y II son muy buenos, por los que esperamos tener los mismos en fase III. Este proyecto es un gran desafío y también conlleva una gran responsabilidad para los investigadores implicados”, asegura Natalini.
✕
Accede a tu cuenta para comentar

Experiencias en el extranjero


