Inmunización
La EMA recomienda la vacuna de Pfizer contra la variante XBB.1.5 de la covid
Señala que adultos y niños a partir de 5 años de edad que requieran inmunizarse deben recibir una dosis única
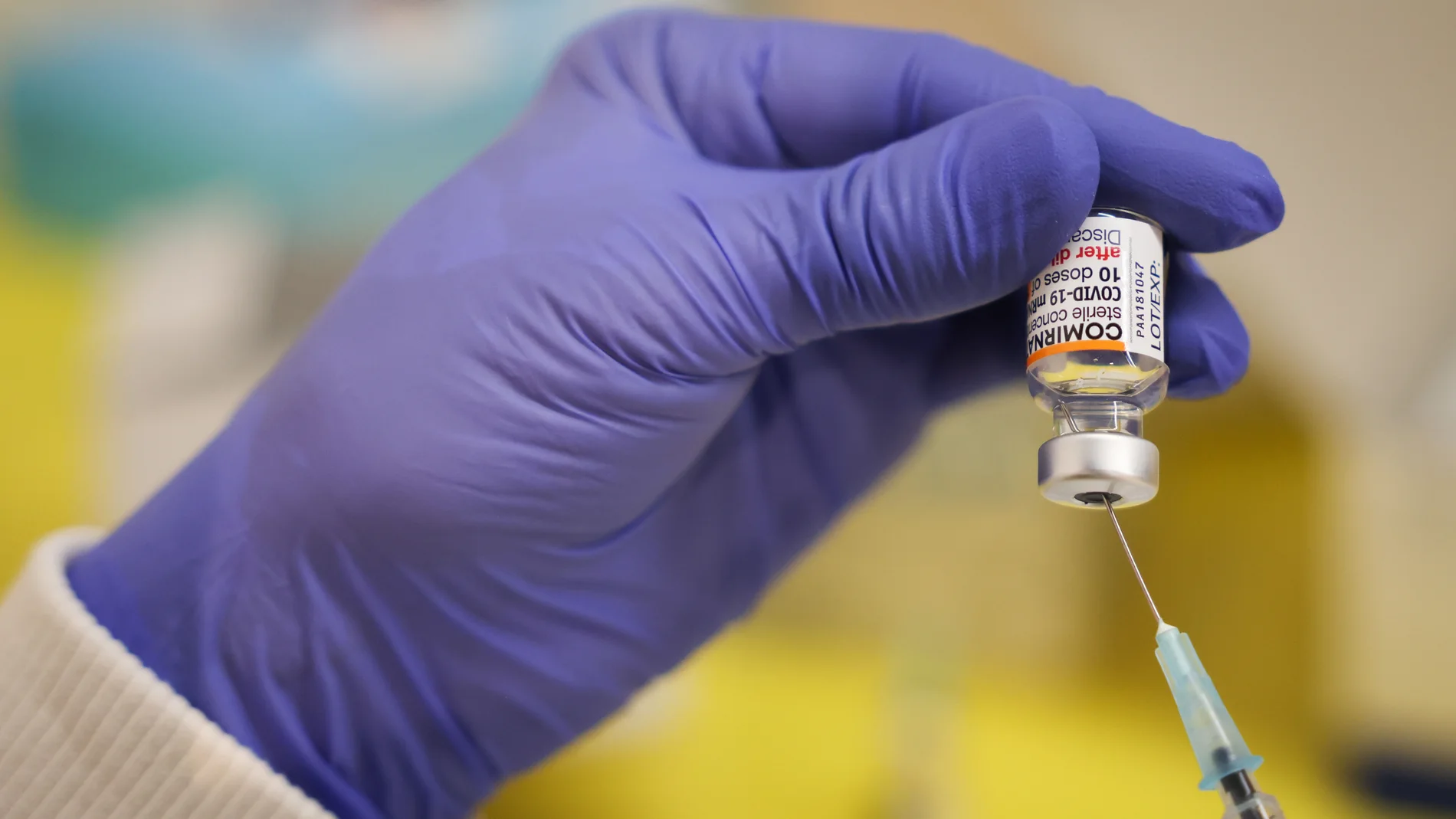
El Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha recomendado autorizar la vacuna adaptada de Pfizer/BioNTech contra la Covid-19 ("Comirnaty") para la subvariante Ómicron XBB.1.5 (también conocida como Kraken).
La vacuna, denominada "Comirnaty Omicron XBB.1.5", se utilizará para prevenir la Covid-19 en adultos y niños a partir de los 6 meses de edad, informa Ep.
De acuerdo con las recomendaciones anteriores de la EMA y del Centro Europeo para la Prevención y el Control de las Enfermedades (ECDC), los adultos y los niños a partir de 5 años de edad que requieran vacunación deben recibir una dosis única, independientemente de su historial de vacunación contra la Covid-19.
Los niños de 6 meses a 4 años de edad pueden recibir una o tres dosis, dependiendo de si han completado un curso de vacunación primaria o han tenido Covid-19.
En su decisión de recomendar la autorización, el CHMP consideró todos los datos disponibles sobre "Comirnaty" y sus otras vacunas adaptadas, incluidos los datos sobre seguridad, eficacia e inmunogenicidad (la eficacia con que desencadenan respuestas inmunitarias). Además, el Comité evaluó nuevos datos de laboratorio que mostraban una fuerte respuesta de la vacuna adaptada contra XBB.1.5 y cepas relacionadas del virus que causa la Covid-19. Se esperan más datos sobre variantes emergentes, que el Comité evaluará cuando estén disponibles.
Efectos secundarios leves
Las vacunas contra la Covid-19 se adaptan para que se ajusten mejor a las variantes circulantes. Esta vacuna se desarrolló para dirigirse a Ómicron XBB, de acuerdo con las recomendaciones de la EMA y el ECDC, así como otros reguladores internacionales y la Organización Mundial de la Salud.
Dado que Ómicron XBB.1.5 está estrechamente relacionada con otras variantes actualmente circulantes, se espera que la vacuna ayude a mantener una protección óptima contra la Covid-19 causada por estas otras variantes, así como por Ómicron XBB.1.5.
Desde la primera autorización de "Comirnaty", las autoridades han adquirido amplios conocimientos sobre la seguridad de la vacuna. Los efectos secundarios suelen ser leves y de corta duración. Incluyen dolor de cabeza, diarrea, dolor articular y muscular, cansancio, escalofríos, fiebre y dolor o hinchazón en el lugar de la inyección. En raras ocasiones pueden producirse efectos secundarios más graves.
La EMA enviará ahora la recomendación del CHMP a la Comisión Europea para que adopte una decisión jurídicamente vinculante en toda la UE. Al igual que con otras vacunas Covid-19, las autoridades nacionales de los Estados miembros de la UE determinarán cómo utilizar esta vacuna en las campañas nacionales de vacunación, teniendo en cuenta factores como las tasas de infección y hospitalización, el riesgo para las personas vulnerables y la disponibilidad de la vacuna.
"Comirnaty" se autorizó por primera vez en la UE en diciembre de 2020, y las versiones adaptadas dirigidas a las cepas BA.1 y BA.4-5 obtuvieron una nueva autorización en septiembre de 2022.
✕
Accede a tu cuenta para comentar

Testimonio gráfico