
Nueva enfermedad
Hallan por primera vez una forma genética de ELA en niños
Por primera vez se apunta a que la ELA puede estar causada por cambios en la metabolización de los lípidos que puede aparecer en la infancia, según publica la revista “Nature Medicine”
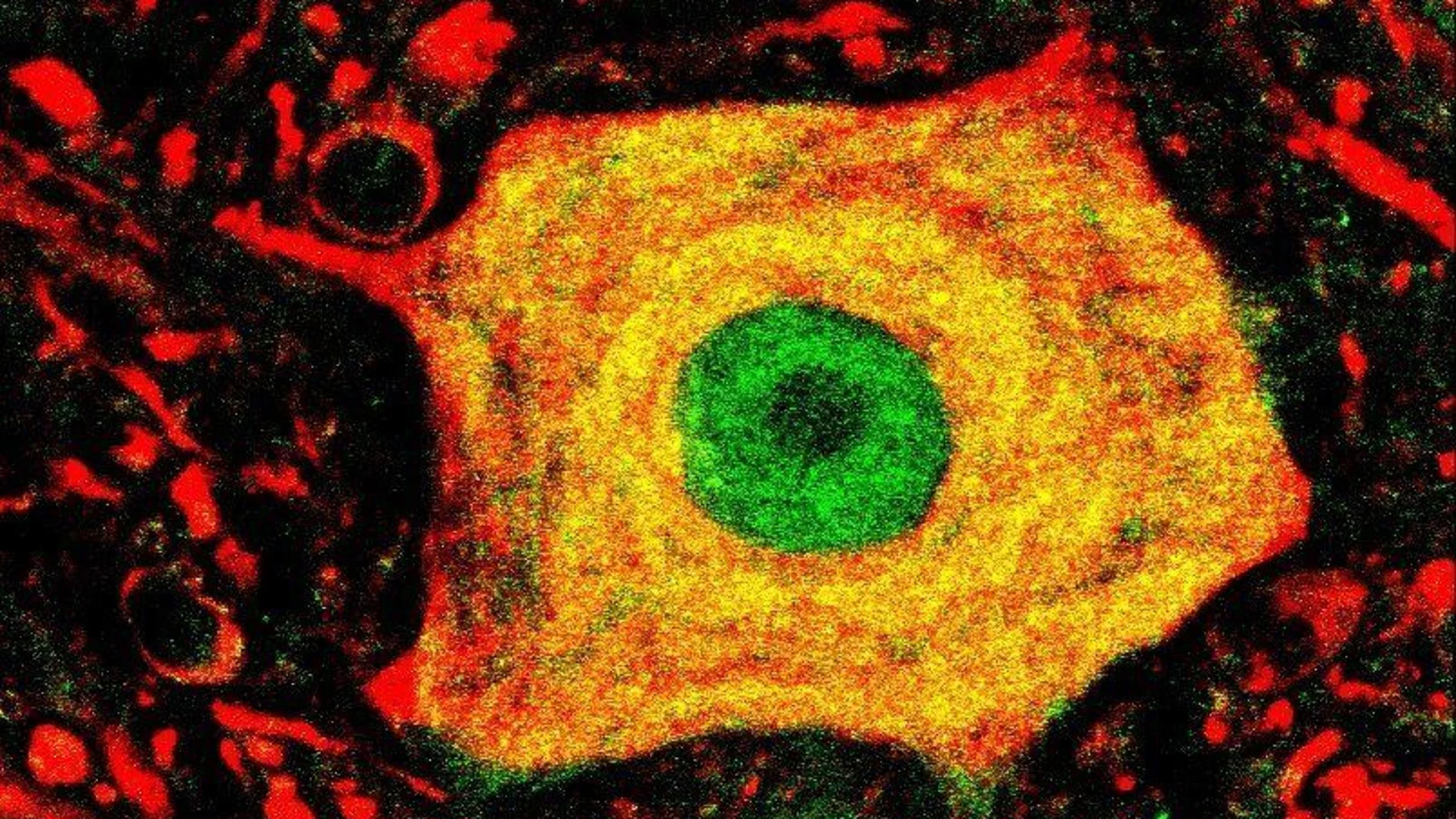
La esclerosis lateral amiotrófica, conocida como ELA, es una patología que ataca a las neuronas del cerebro y a la médula espinal encargada de controlar el movimiento, convirtiéndose en una enfermedad neurodegenerativa muy invalidante que tradicionalmente afecta a adultos jóvenes. Pero también puede atacar a los menores, tal y como acaba de confirmar un estudio dirigido por científicos de los Institutos Nacionales de la Salud de Estados Unidos y la Universidad de Servicios Uniformados realizado en 11 pacientes con incógnitas médicas que han descubierto una forma nueva y única de esclerosis lateral amiotrófica (ELA) que comienza en la infancia, tal y como publica la revista científica “Nature Medicine”.
A diferencia de lo que ocurre habitualmente en los casos de ELA, la enfermedad comenzó a atacar a estos pacientes durante la infancia y empeoró más lentamente de lo habitual. En este caso, la patología se vinculó a un gen, denominado SPTLC1, que forma parte del sistema de producción de grasa del organismo, por lo que los resultados preliminares sugerían que apagar genéticamente la actividad de SPTLC1 podría convertirse en una estrategia eficaz para combatir este tipo de ELA.
“La ELA es una enfermedad paralizante y a menudo mortal que suele afectar a personas de mediana edad. Hemos descubierto que una forma genética de la enfermedad también puede amenazar a los niños. Nuestros resultados demuestran por primera vez que la ELA puede estar causada por cambios en el modo en que el organismo metaboliza los lípidos”, explica el doctor Carsten Bönnemann, investigador principal del Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares (NINDS) de los Institutos Nacionales de Salud (NIH) y autor principal del estudio, quien hace hincapié en que “esperamos que estos resultados ayuden a los médicos a reconocer esta nueva forma de ELA y conduzcan al desarrollo de tratamientos que mejoren la vida de estos niños y adultos jóvenes. Confiamos en que nuestros resultados puedan proporcionar nuevas pistas para entender y tratar otras formas de la enfermedad”.
El doctor Bönnemann dirige un equipo de investigadores que utiliza técnicas genéticas avanzadas para resolver algunos de los trastornos neurológicos infantiles más misteriosos del mundo. En este estudio, el equipo descubrió que 11 de estos casos tenían ELA vinculada a variaciones en la secuencia de ADN de SPLTC1, un gen responsable de la fabricación de una clase diversa de grasas llamadas esfingolípidos. Además, el equipo colaboró con científicos de los laboratorios dirigidos por la doctora Teresa M. Dunn, profesora y catedrática de la USU, y el doctor Thorsten Hornemann, de la Universidad de Zúrich (Suiza). Juntos no sólo encontraron pistas sobre cómo las variaciones en el gen SPLTC1 conducen a la ELA, sino que también desarrollaron una estrategia para contrarrestar estos problemas.
Casos clínicos
El estudio comenzó con Claudia Digregorio, una joven de la región italiana de Apulia. Como muchos de los demás pacientes, Claudia necesitaba una silla de ruedas para desplazarse y un tubo de traqueotomía implantado quirúrgicamente para ayudarle a respirar. Los exámenes neurológicos realizados por el equipo revelaron que tanto ella como los demás pacientes presentaban muchos de los rasgos distintivos de la ELA, como músculos gravemente debilitados o paralizados. Además, los músculos de algunos pacientes mostraban signos de atrofia cuando se examinaban al microscopio o con escáneres no invasivos. Sin embargo, esta forma de ELA parecía ser diferente. A la mayoría de los pacientes se les diagnostica la ELA en torno a los 50 o 60 años de edad. La enfermedad empeora tan rápidamente que los pacientes suelen morir entre tres y cinco años después del diagnóstico. En cambio, los síntomas iniciales, como la marcha de los dedos del pie y la espasticidad, aparecieron en estos pacientes alrededor de los cuatro años de edad. Además, al final del estudio, los pacientes habían vivido entre cinco y 20 años más.
“Estos jóvenes pacientes tenían muchos de los problemas de las neuronas motoras superiores e inferiores que son indicativos de la ELA, lo que hizo que estos casos fueran únicos fue la edad temprana de inicio y la progresión más lenta de los síntomas. Esto nos hizo preguntarnos qué subyacía en esta forma distinta de ELA”, reconoce el doctor Payam Mohassel, investigador clínico de los NIH y autor principal del estudio.
Las primeras pistas surgieron del análisis del ADN de los pacientes. Los investigadores utilizaron herramientas genéticas de nueva generación para leer los exomas de los pacientes, las secuencias de ADN que contienen las instrucciones para fabricar proteínas. En concreto, descubrieron que los pacientes presentaban cambios llamativos en la misma porción estrecha del gen SPLTC1. Cuatro de los pacientes heredaron estos cambios de uno de sus padres. Mientras tanto, los otros seis casos parecían ser el resultado de lo que los científicos llaman mutaciones “de novo” en el gen. Este tipo de mutaciones puede producirse espontáneamente cuando las células se multiplican rápidamente antes o poco después de la concepción. Al principio, el equipo pensó que las mutaciones causantes de la ELA que descubrieron podrían producir problemas similares. Sin embargo, los análisis de sangre de los pacientes no mostraron signos de los esfingolípidos dañinos.
Durante décadas, el equipo del doctor Dunn había estudiado el papel de los esfingolípidos en la salud y la enfermedad. Con la ayuda del equipo de Dunn, los investigadores volvieron a examinar las muestras de sangre de los pacientes con ELA y descubrieron que los niveles de los esfingolípidos típicos eran anormalmente altos. Esto sugería que las mutaciones de la ELA potenciaban la actividad de los SPT. Así, se observaron resultados similares cuando los investigadores programaron neuronas cultivadas en placas de Petri para que fueran portadoras de las mutaciones causantes de la ELA en SPLTC1.
Estudios anteriores han sugerido que la suplementación con serina puede ser un tratamiento eficaz para la HSAN1. Basándose en sus resultados, los autores de este estudio recomendaron evitar los suplementos de serina al tratar a los pacientes con ELA. A continuación, el equipo del doctor Dunn realizó una serie de experimentos que demostraron que las mutaciones causantes de la ELA impiden que otra proteína llamada ORMDL inhiba la actividad de la SPT.
“Nuestros resultados sugieren que estos pacientes con ELA viven esencialmente sin un freno a la actividad de la SPT. La SPT está controlada por un bucle de retroalimentación. Cuando los niveles de esfingolípidos son altos, las proteínas ORMDL se unen a la SPT y la frenan. Las mutaciones que estos pacientes portan cortocircuitan esencialmente este bucle de retroalimentación. Pensamos que restaurar este freno podría ser una buena estrategia para tratar este tipo de ELA”, advierte Dunn, Para probar esta idea, el equipo de Bönnemann creó pequeñas cadenas de ARN de interferencia diseñadas para desactivar los genes mutantes SPLTC1 encontrados en los pacientes. Los experimentos con las células de la piel de los pacientes demostraron que estas cadenas de ARN reducían los niveles de actividad del gen SPLTC1 y restablecían los niveles de esfingosina a la normalidad. “Estos resultados preliminares sugieren que podríamos utilizar una estrategia de silenciamiento génico de precisión para tratar a los pacientes con este tipo de ELA. Además, también estamos explorando otras formas de pisar el freno que frena la actividad de la SPT. Nuestro objetivo final es traducir estas ideas en tratamientos eficaces para nuestros pacientes que actualmente no tienen opciones terapéuticas”, concluye Bonnemann.
✕
Accede a tu cuenta para comentar




