
Oncología
Quimioterapia en desescalada: una realidad de cada vez más pacientes con cáncer de mama
A los biomarcadores y pruebas genéticas, como la determinación de DNA circular tumoral, se suman terapias farmacológicas que hacen que el uso de la quimio en muchos casos sea innecesario
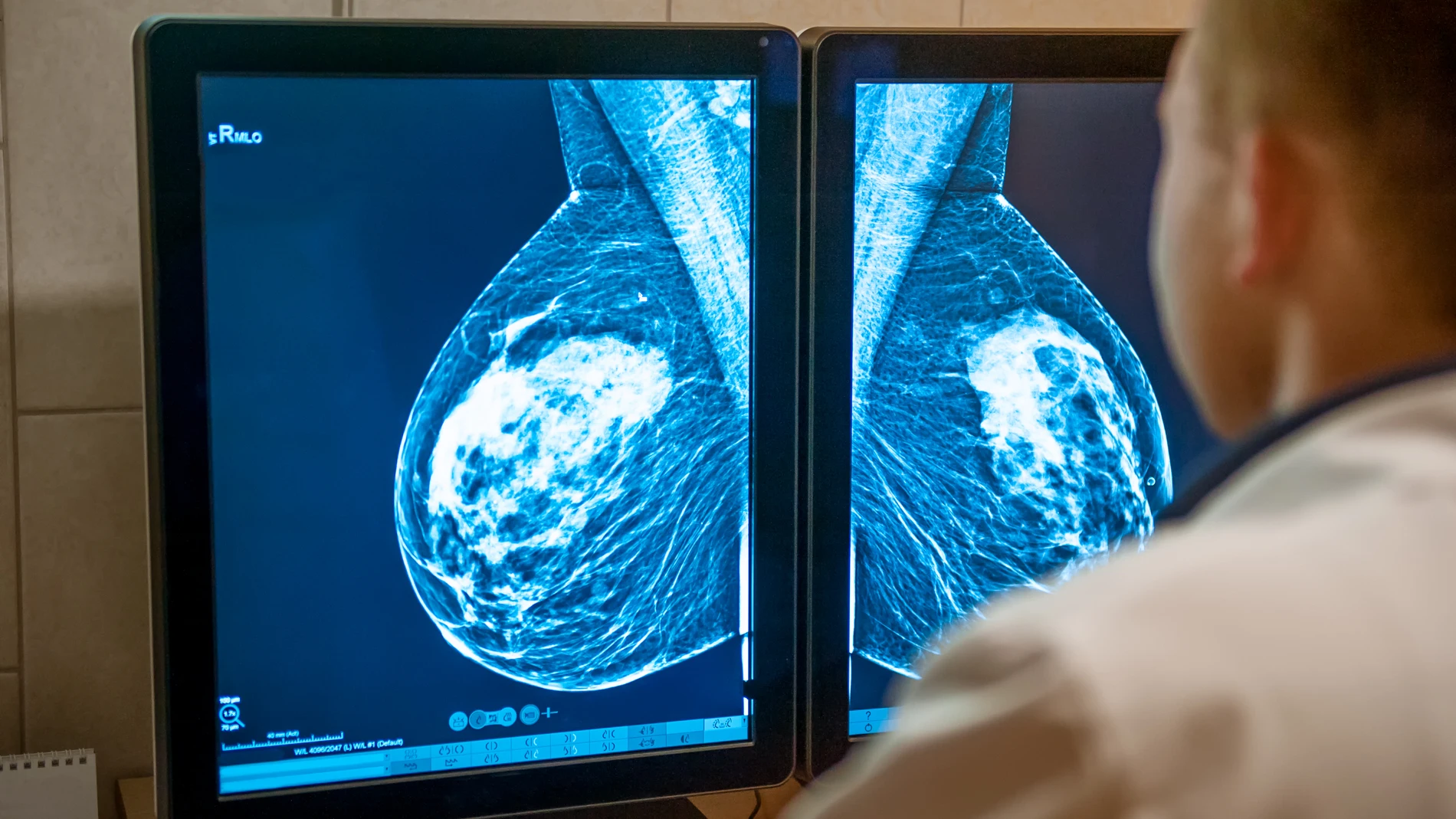
Cada hora, 4,3 mujeres serán diagnosticadas este año de cáncer de mama en España. No todas necesitarán quimioterapia para reducir el riesgo de que el cáncer reaparezca. De hecho, aunque la quimioterapia sigue siendo un tratamiento eficaz y necesario para algunos casos, las pautas de tratamiento han cambiado y van a seguir cambiando, de modo que no se recomienda hoy a tantas personas como hace 20 años y en el futuro se indicará a muchas menos.
«Cuando empecé a estudiar, prácticamente cualquier paciente operado de cáncer de mama recibía un tratamiento de quimioterapia. Hoy, te diría que únicamente un 60% sigue recibiendo quimio antes o después. Es una diferencia abismal, y estamos dando pasos para que ese porcentaje sea cada vez menor», explica Tomás Pascual, miembro de la junta directiva de Solti y oncólogo médico en el Hospital Clínico de Barcelona.
Como explica César A. Rodríguez, presidente de la Sociedad Española de Oncología Médica (SEOM), «en la actualidad, el uso de quimioterapia no constituye ya un tratamiento estándar en muchos casos de cáncer de mama. Es una estrategia más incluida dentro de un arsenal terapéutico muy amplio que solo se emplea en aquellas indicaciones en las que ha demostrado un beneficio tanto en enfermedad temprana, disminuyendo el riesgo de recaída, como en enfermedad avanzada, aumentando en algunos casos la supervivencia».
Así, la quimioterapia puede utilizarse para disminuir el riesgo de recaída y, por tanto, ayudar a vivir más tiempo. Pero en ciertos casos, cada vez más, existen mejores opciones que destruyen el cáncer, sin sufrir pérdida de cabello, náuseas, fatiga, mayor riesgo de infecciones (debido a una menor cantidad de glóbulos blancos), etc.
Ahora bien, aunque «su uso ha disminuido(en el caso del luminal ya mucho menos de la mitad de las pacientes recibe quimio) y disminuirá aún más, seguiremos usando quimioterapia, aunque probablemente cada vez menos como tratamiento único, y más en combinación con inmunoterapia, anticuerpos monoclonales o dentro de nuevos tratamientos, como sucede con los anticuerpos conjugados, que son moléculas que incluyen un anticuerpo monoclonal y una molécula de quimioterapia unida al mismo que permite una administración más selectiva y con menos efectos secundarios», explica Rodríguez.
Como cada vez hay tratamientos más efectivos, lo que se busca, según Pascual, «es que sean menos tóxicos, y, por lo tanto, lo que estamos haciendo es relegar los tratamientos de la quimioterapia clásica a escenarios más acotados».
En este sentido, «los primeros resultados que hemos presentado del estudio ‘‘Ribolaris’’ en el congreso anual de la Sociedad Europea para la Medicina Oncológica (ESMO) revelan que más de mitad de los pacientes con cáncer de mama con receptores hormonales positivos de alto riesgo podrían evitar la quimioterapia cuando se tratan con ribociclib y terapia endocrina».
El ensayo ha contado 686 pacientes intervenidas quirúrgicamente (de las 1.100 en total), de las cuales 361 (52,6%) de las pacientes con cáncer de mama con receptores hormonales positivos y HER2 negativo (HR+/HER2−) de alto riesgo alcanzaron un perfil de bajo riesgo de recurrencia tras seis meses de tratamiento neoadyuvante con ribociclib y letrozol, superando la expectativa inicial del 40%.
La hipótesis del estudio es que, en pacientes recién diagnosticadas, iniciar el tratamiento con ribociclib y terapia endocrina puede revelar, en el momento de la cirugía, qué tumores responden tan bien, que la quimioterapia podría no ser necesaria, cuando el tratamiento estándar para estas pacientes ahora mismo sería, además de la cirugía, «quimioterapia, terapia hormonal e inhibidor de ciclinas durante tres años».
Para el estudio, los participantes tenían el tipo de tumor hormonal descrito «en estadio 2, localizado en la mama. Aunque tenga poca afectación axilar, tratamos a las pacientes seis meses con una terapia endocrina y un inhibidor de CDK –ribociclib–, que lo que hace es bloquear justamente las ciclinas antes de la cirugía», detalla Pascual.
Y los resultados del estudio académico liderado por Solti, en colaboración con UniCancer y con el apoyo de Novartis, hablan por sí solos. «La gran mayoría de tumores –prosigue– responden, es decir, el tumor se hace más pequeño, les baja la proliferación (de células cancerígenas) y después de estos seis meses de tratamiento operamos y estudiamos ese tumor».
Esta muestra extraída permite saber qué pacientes responden y qué pacientes responden muy bien, que son aquellos en los que vemos que claramente se le ha inhibido completamente la proliferación del tumor y que ha bajado mucho el riesgo de recaída».
Pues bien, en el caso de esas pacientes a las que baja mucho el riesgo de recaída y que baja mucho la proliferación, «continuamos con el tratamiento y en aquellas pacientes que aunque hayan respondido, es decir, su tumor se haya hecho más pequeño pero seguimos viendo que sigue habiendo algo de proliferación, pues lo que hacemos es darles el tratamiento de quimioterapia que hubiesen recibido previamente», detalla el doctor.
El siguiente paso es confirmar estos resultados en toda la cohorte y evaluar si siguen evolucionando favorablemente sin quimioterapia.
Preguntado sobre si las mujeres que acaban recibiendo quimio después por no responder tanto como se esperaba tendrán los mismos resultados que si se hubieran dado quimio antes de la cirugía, Pascual reconoce que no puede dar este dato, ya que el estudio no lo analiza, pero «fuera del estudio actual, viendo el tratamiento del cáncer de mama desde sus inicios y hasta ahora, la eficacia de poner el tratamiento antes o después de la cirugía, a nivel de supervivencia es igual».
Pero no solo sucede esto en cáncer de mama. Aunque el cáncer de mama «va siempre un poco adelantado respecto a otros tumores, los pacientes con cáncer de pulmón metastásico hoy solo reciben tratamiento con inmunoterapia en primera línea y en el caso del cáncer de colon hay pacientes que, tras la cirugía, por medio de un test de la determinación de DNA circular tumoral, no se vea ctDNA (que hubiera significaría que las células cancerosas aún están creciendo y muriendo, en algún lugar del cuerpo, incluso a niveles bajos) esos pacientes podrían omitir la quimioterapia de forma segura», explica Pascual.
Perfiles de expresión genética
A esta técnica de detección de ctDNA, que puede ser útil para detectar un tumor y orientar qué tratamiento es mejor para un paciente, hay que sumar que ya existen biomarcadores que predicen qué pacientes no responderán a la quimioterapia contra el cáncer. Y es que, aunque este tratamiento con productos químicos busca acabar con las células tumorales mediante fármacos, no siempre da buen resultado.
De hecho, «se estima que entre un 20 y un 50% de pacientes con cáncer (no solo de mama) no responden a estos fármacos», según un comunicado del Centro Nacional de Investigaciones Oncológicas (CNIO). Es decir, que sufrirán los efectos secundarios causados por la quimioterapia, sin tener beneficio clínico.
En este sentido, este centro de investigación ha desarrollado un método que predice en qué pacientes no serán eficaces los tratamientos estándar con quimioterapias de uso frecuente, basados en los compuestos con platino, taxanos y antraciclinas.
Un nuevo método que se suma a las plataformas genómicas o perfiles de expresión génica existentes, «que permiten identificar pacientes con tumores de bajo riesgo de recaída y sin beneficio en el uso de quimioterapia han sido sin duda uno de los grandes avances en el tratamiento del cáncer de mama en estadios precoces de los últimos 10-15 años. También en enfermedad avanzada el empleo de nuevos biomarcadores permite el uso de determinados tratamientos con menor toxicidad y con mayor probabilidades de respuesta», destaca el presidente de SEOM.
✕
Accede a tu cuenta para comentar




